Слайд 2

Повторение: виды химической связи
какие атомы МОГУТ принимать участие в образовании ковалентной
связи: H, Cl, Na, F, S, Li, O, N?
какой тип связи в соединении с симметрично расположенной общей е-парой?
Что происходит с электронами Ме, когда атомы Ме образуют ионную связь?
какой тип связи возникает между атомами Zn и Cu в латуни?
Слайд 3

Слайд 4

Водородная связь
возникает между какими атомами соседних молекул вещества: N, S, Cl,
Na, H, I, F, Fr, He, O;
на что влияет водородная связь между молекулами вещества;
приведите примеры веществ, где есть водородная связь
Слайд 5

Кристаллические вещества
встречаются основном в твердом состоянии,
характеризуются упорядоченным расположением частиц,
результатом мысленного соединения
точек расположения частиц в кристалле является КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА:
узлы решетки – точки в пространстве, где расположены частицы вещества;
ребра решетки – линии соединения этих точек, связи между частицами вещества
Слайд 6

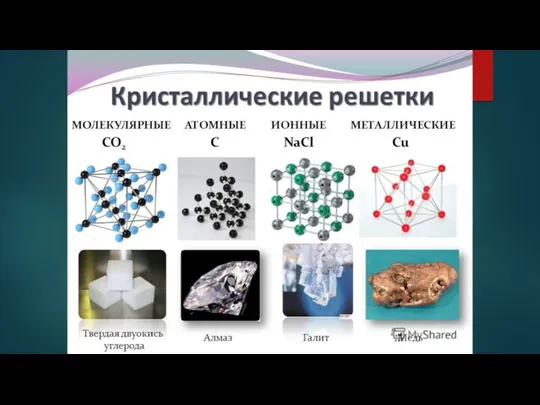
Типы кристаллических решеток
Ионная
Атомная
Металлическая
Молекулярная
физические свойства вещества зависят от:
природы частиц вещества
вида химической
связи между частицами
Слайд 7
Слайд 8

Ионная кристаллическая решетка
Слайд 9
Слайд 10

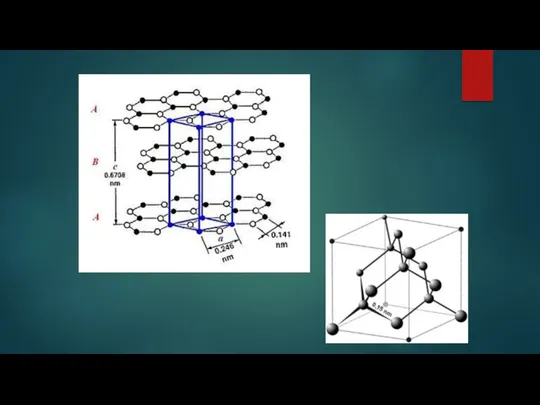
Атомная кристаллическая решетка
Слайд 11

Металлическая кристаллическая решетка
в узлах решетки находятся __________
тип связи между частицами вещества
в кристалле ________________________
твердые вещества (кроме Hg), пластичные, с металлическим блеском, в твердом состоянии проводят электрический ток
примеры: все Ме и их сплавы (латунь, бронза, мельхиор, дюралюмин)
Слайд 12

Молекулярная кристаллическая решетка











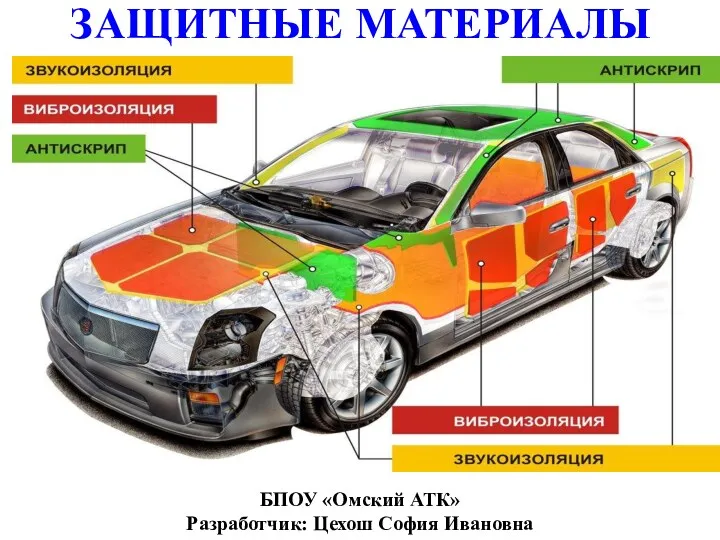 Защитные материалы
Защитные материалы Органічна хімія, частина 1
Органічна хімія, частина 1 Методы восстановления и окисления
Методы восстановления и окисления Мыло. Его состав и моющее действие. Синтетические моющие средства
Мыло. Его состав и моющее действие. Синтетические моющие средства Химическая термодинамика. Термохимия
Химическая термодинамика. Термохимия Классификация и номенклатура органических соединений. (Лекция 1)
Классификация и номенклатура органических соединений. (Лекция 1) Кремний и его соединения
Кремний и его соединения Химиялық элементтердің тірі және өлі табиғатта таралуы
Химиялық элементтердің тірі және өлі табиғатта таралуы Кількість речовини. Моль - одиниця кількості речовини. Число Авогадро
Кількість речовини. Моль - одиниця кількості речовини. Число Авогадро Получение полимеров из низкомолекулярных соединений
Получение полимеров из низкомолекулярных соединений Характеристика химического элемента по его положению в периодической системе элементов Д.И.Менделеева
Характеристика химического элемента по его положению в периодической системе элементов Д.И.Менделеева Кислородсодержащие соединения серы. Оксиды, кислоты, соли
Кислородсодержащие соединения серы. Оксиды, кислоты, соли Классификация химических реакций
Классификация химических реакций Припекание взаимно растворимых твердых тел
Припекание взаимно растворимых твердых тел Химическая промышленность. Минеральные удобрения
Химическая промышленность. Минеральные удобрения Классификация химических реакций
Классификация химических реакций Качественные реакции на функциональные группы. Классификация функциональных групп
Качественные реакции на функциональные группы. Классификация функциональных групп Нефть. Углеводороды
Нефть. Углеводороды Спирты. Классификация
Спирты. Классификация Ненасыщенные (непредельные) углеводороды. Алкены (олефины)
Ненасыщенные (непредельные) углеводороды. Алкены (олефины) Тему Соли. Нитрат серебра(I) AgNO3
Тему Соли. Нитрат серебра(I) AgNO3 Витамины
Витамины Искусственная радиоактивность. Ядерное оружие и его поражающие факторы
Искусственная радиоактивность. Ядерное оружие и его поражающие факторы Sources of alkanes and cycloalkanes. Crude oil
Sources of alkanes and cycloalkanes. Crude oil Photocatalysts based on AgCl / Ag nanocomposites
Photocatalysts based on AgCl / Ag nanocomposites Синтетические топлива
Синтетические топлива Вещества и тела. Состояния веществ. Смеси
Вещества и тела. Состояния веществ. Смеси Модифицированные природные полимеры. Их свойства
Модифицированные природные полимеры. Их свойства