Содержание
- 2. 1. Классификация химических реакций по кинетическим признакам. 2. Порядок и молекулярность реакции. 3. Роль катализа в
- 3. Время протекания реакции скорость реакции кинетика «kinẽtikos”, что означает “движущийся”. Кинетика – раздел физической химии, изучающий
- 4. В химической кинетике взаимодействия классифицируют или по признаку молекулярности реакции, или по признаку порядка реакции. Молекулярность
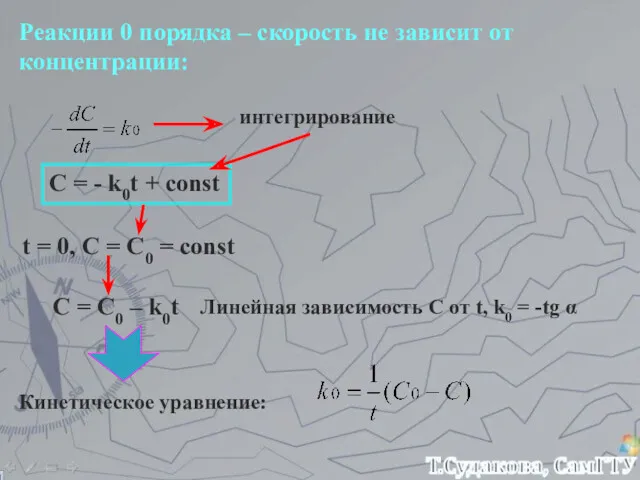
- 5. Реакции 0 порядка – скорость не зависит от концентрации: интегрирование C = - k0t + const
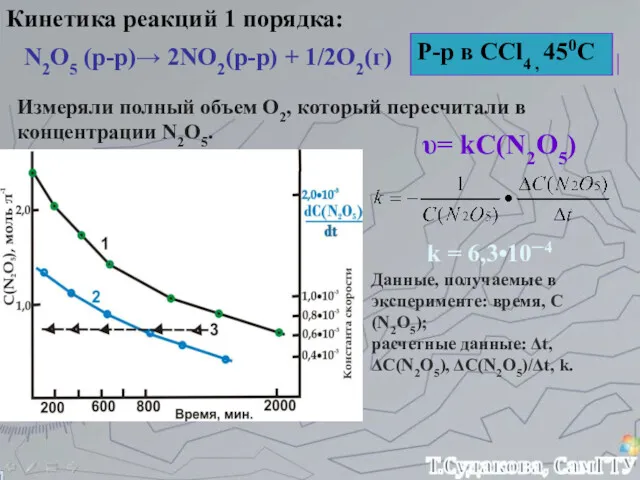
- 6. Кинетика реакций 1 порядка: N2O5 (р-р)→ 2NO2(р-р) + 1/2O2(г) Р-р в CCl4 , 450С Измеряли полный
- 7. Реакции 2 порядка: С1 и С2 – концентрации реагентов в момент времени t. Если С1 =
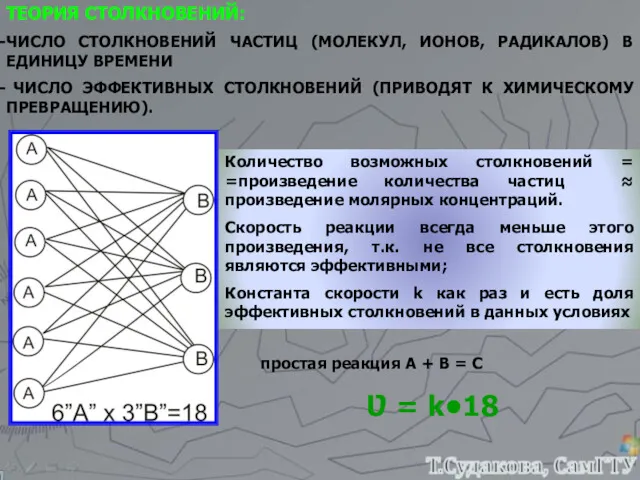
- 8. ТЕОРИЯ СТОЛКНОВЕНИЙ: ЧИСЛО СТОЛКНОВЕНИЙ ЧАСТИЦ (МОЛЕКУЛ, ИОНОВ, РАДИКАЛОВ) В ЕДИНИЦУ ВРЕМЕНИ ЧИСЛО ЭФФЕКТИВНЫХ СТОЛКНОВЕНИЙ (ПРИВОДЯТ К
- 9. Основной закон химической кинетики (ОЗХК) описывает зависимость скорости реакции от концентрации реагирующих веществ:скорость химической реакции в
- 10. Гомогенные реакции – реакции, в которых все реагенты находятся в одном агрегатном состоянии разложение 2N2O5 (г)
- 11. Скорость химической реакции определяют экспериментально. По полученным результатам эксперимента строят кинетическую кривую - график изменения концентрации
- 12. Для реакции: А + 2В = 3С υ = Для реакции: H2 + I2 = 2HI
- 13. Факторы, влияющие на скорость реакции: - концентрация реагентов, - температура, - физическое состояние реагентов, - наличие
- 14. Важное замечание! Концентрация конденсированной фазы не включается в выражение ЗДМ, т.к. она является постоянной величиной. Пример:
- 15. Для реакции вида аА + bB = cC закон действующих масс выражается формулой Ʋ = k
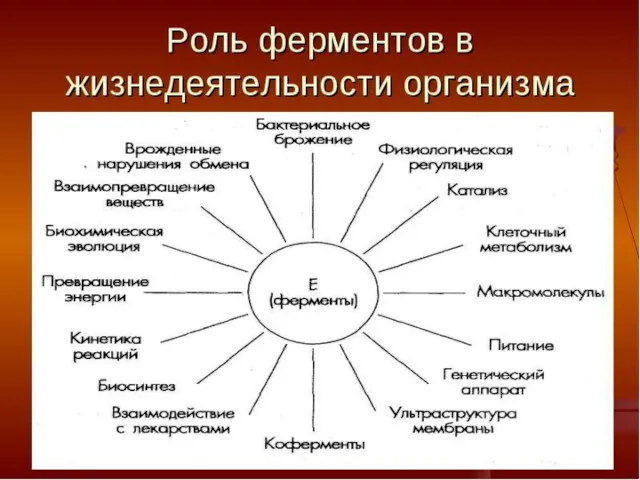
- 16. Уравне́ние Михаэ́лиса — Ме́нтен — основное уравнение ферментативной кинетики, описывает зависимость скорости реакции, катализируемой ферментом, от
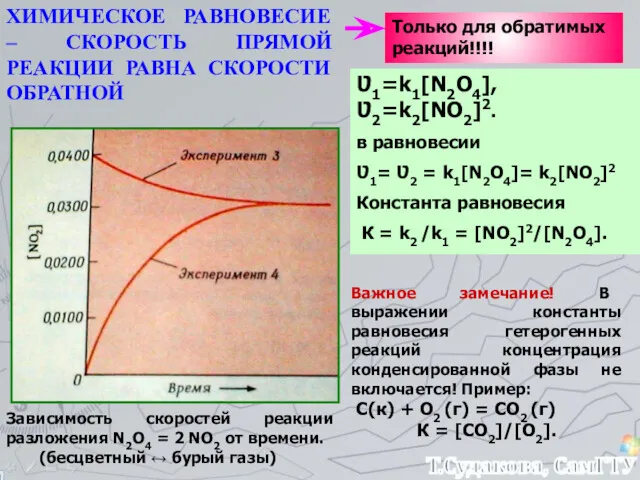
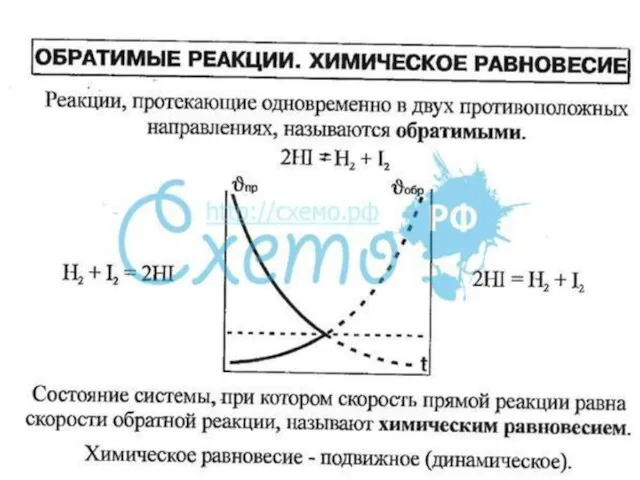
- 17. Химическое равновесие — состояние химической — состояние химической системы, в котором протекает одна или несколько химических
- 18. Зависимость скоростей реакции разложения N2О4 = 2 NО2 от времени. (бесцветный ↔ бурый газы) ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 22. Катализатор (по определению В. Оствальда 1905г.) – вещество, которое изменяет скорость химической реакции, не изменяя ее
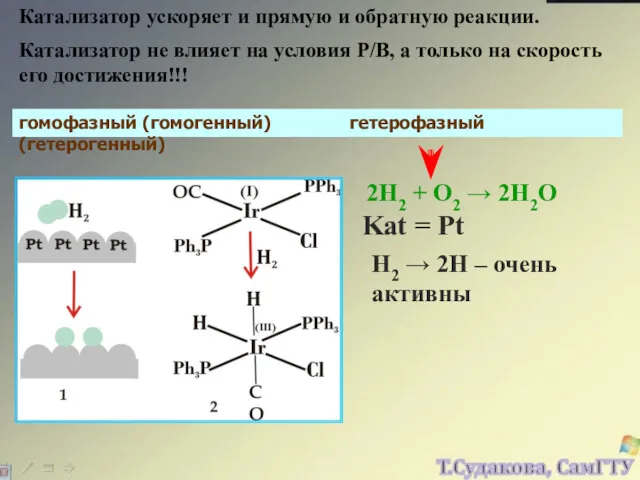
- 23. Катализатор ускоряет и прямую и обратную реакции. Катализатор не влияет на условия Р/В, а только на
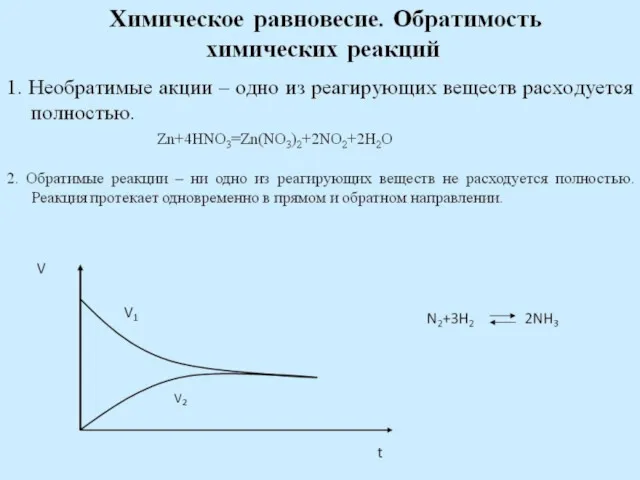
- 24. Обрати́мые реа́кции — химические реакции, протекающие одновременно в двух противоположных направлениях (прямом и обратном), протекает до
- 28. Конста́нта равнове́сия — величина, определяющая для данной химической реакции — величина, определяющая для данной химической реакции
- 29. Для реакции в смеси идеальных газовДля реакции в смеси идеальных газов константа равновесия может быть выражена
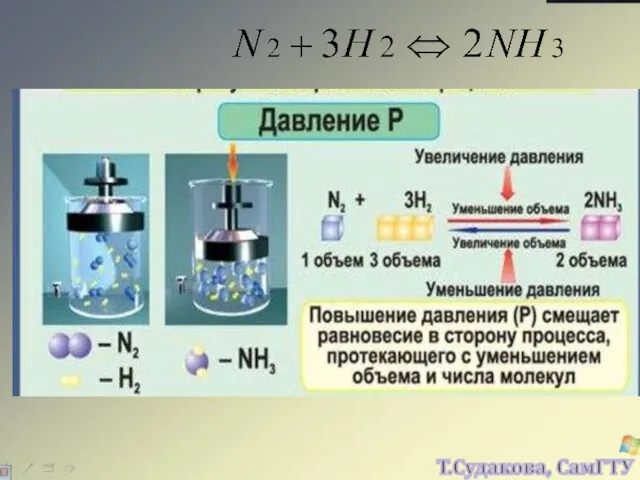
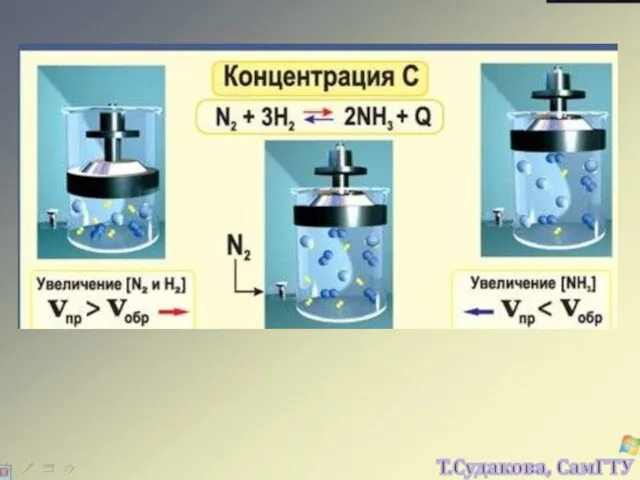
- 30. Изменение любого фактора, могущего влиять на состояние химического равновесия, вызывает в системе реакцию, стремящуюся противодействовать производимому
- 31. Ленский А.С. «Введение в бионеорганическую и биофизическую химию» Кемпбел Дж. Современная общая химия. В трех томах.
- 33. Скачать презентацию




















 Types of chemical bonds in crystals
Types of chemical bonds in crystals Индикаторные ошибки кислотно-основного титрования
Индикаторные ошибки кислотно-основного титрования Подгруппа азота
Подгруппа азота Материаловедение. Контрольная работа
Материаловедение. Контрольная работа Вода - розчинник. Урок 41
Вода - розчинник. Урок 41 Щелочные металлы
Щелочные металлы Жорсткість води і методи її усунення. 11 клас
Жорсткість води і методи її усунення. 11 клас Тағам қоспалары
Тағам қоспалары Оксиды в минералогии
Оксиды в минералогии Классификация минералов по химическому принципу. Занятие 14
Классификация минералов по химическому принципу. Занятие 14 Закон сохранения массы вещества. Уравнения химических
Закон сохранения массы вещества. Уравнения химических Строение и свойства циклоалканов
Строение и свойства циклоалканов Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Галогены
Галогены Алюминий и его соединения
Алюминий и его соединения Решение экспериментальных задач по теме Металлы и их соединения. Практическая работа №4
Решение экспериментальных задач по теме Металлы и их соединения. Практическая работа №4 Chemistry of Coordination Compounds
Chemistry of Coordination Compounds Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью
Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью Знаки химических элементов. Химические формулы. Химический диктант
Знаки химических элементов. Химические формулы. Химический диктант kremniy
kremniy Соли, их классификация и свойства
Соли, их классификация и свойства Коллоидная химия
Коллоидная химия Тема 6-Альдегиды и кетоны
Тема 6-Альдегиды и кетоны Хімія і здоров'я людини
Хімія і здоров'я людини Особенности строения соединений органической химии. 10 класс
Особенности строения соединений органической химии. 10 класс Металлы главных подгрупп
Металлы главных подгрупп 20230419_soli
20230419_soli Агрегатные состояния вещества
Агрегатные состояния вещества