Содержание
- 2. Содержание: Лекция 1 Кристалл. Основные законы кристаллографии……...3 Лекция 2 Кристаллографические категории и сингонии……...18 Лекция 3 Элементы
- 3. Лекция 1 Кристалл. Основные законы кристаллографии. Кристаллография, основные понятия. Свойства кристаллических веществ. Кристаллическое строение. Дефекты кристаллического
- 4. Кристалл. Основные законы кристаллографии Кристаллография — это наука об атомно-молекулярном строении, симметрии, физических свойствах, образовании и
- 5. Кристалл. Основные законы кристаллографии Кристаллы- (от греч. «кристаллос» — лед) это твёрдые тела, в которых атомы
- 6. Кристалл. Основные законы кристаллографии Основные свойства кристаллического вещества Однородность Анизотропность Способность самоограняться Минимальная внутренняя энергия Статичность
- 7. Элементарная трансляция или период идентичности - это кратчайшее из возможных расстояний между одинаковыми точками в ряду
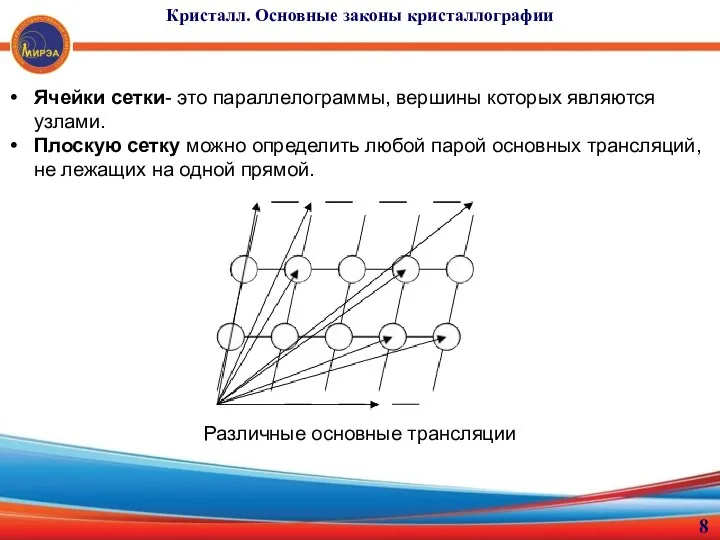
- 8. Ячейки сетки- это параллелограммы, вершины которых являются узлами. Плоскую сетку можно определить любой парой основных трансляций,
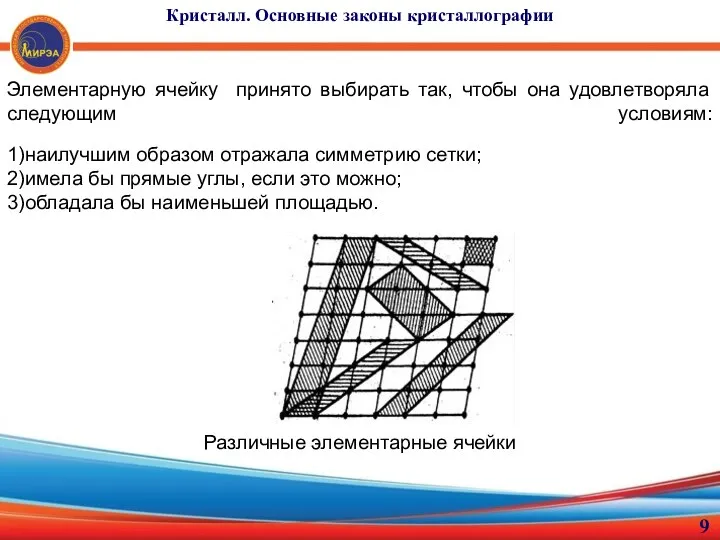
- 9. Элементарную ячейку принято выбирать так, чтобы она удовлетворяла следующим условиям: 1)наилучшим образом отражала симметрию сетки; 2)имела
- 10. Типы элементарных ячеек a – примитивная; b – объемноцентрированная; c – базоцентрированная; d – гранецентрированная. Кристалл.
- 11. Кристалл. Основные законы кристаллографии Кристаллическая решетка представляет собой абстрактный математический образ, позволяющий фиксировать расположение частиц в
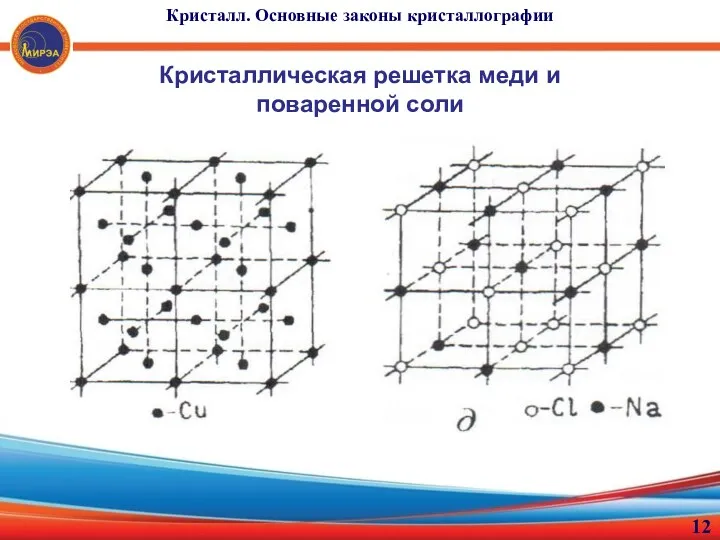
- 12. Кристалл. Основные законы кристаллографии Кристаллическая решетка меди и поваренной соли
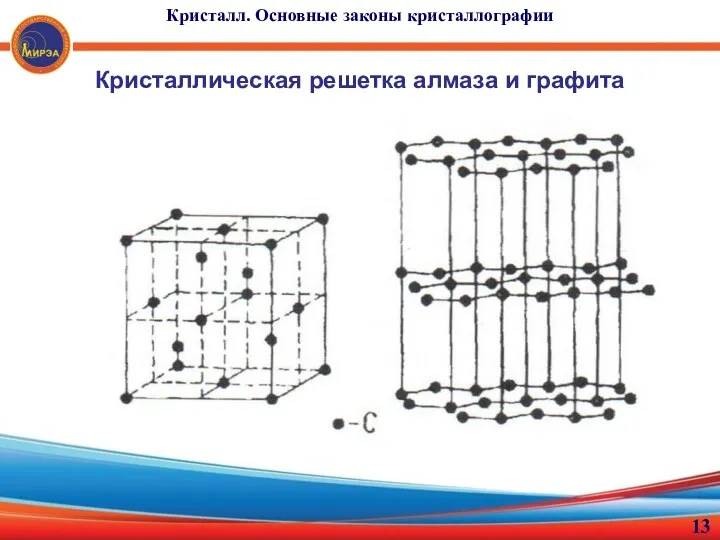
- 13. Кристалл. Основные законы кристаллографии Кристаллическая решетка алмаза и графита
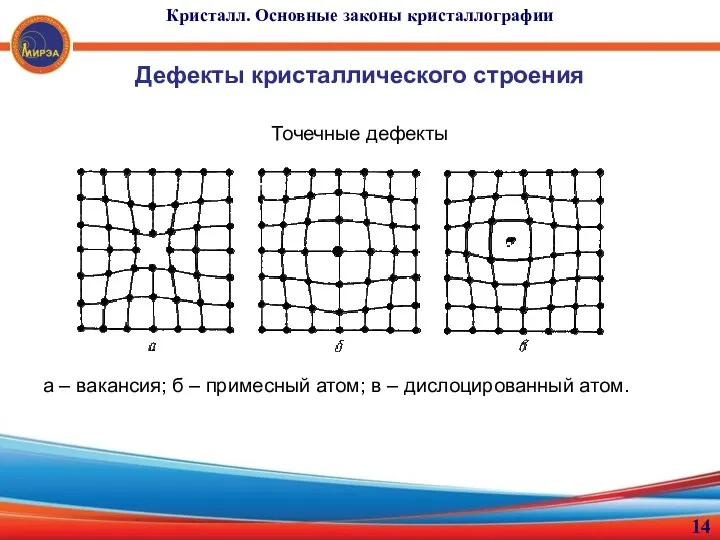
- 14. Кристалл. Основные законы кристаллографии Дефекты кристаллического строения Точечные дефекты а – вакансия; б – примесный атом;
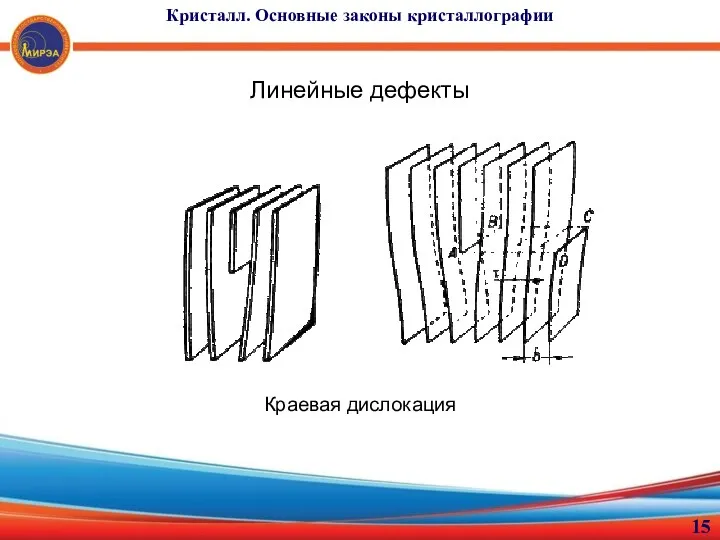
- 15. Кристалл. Основные законы кристаллографии Линейные дефекты Краевая дислокация
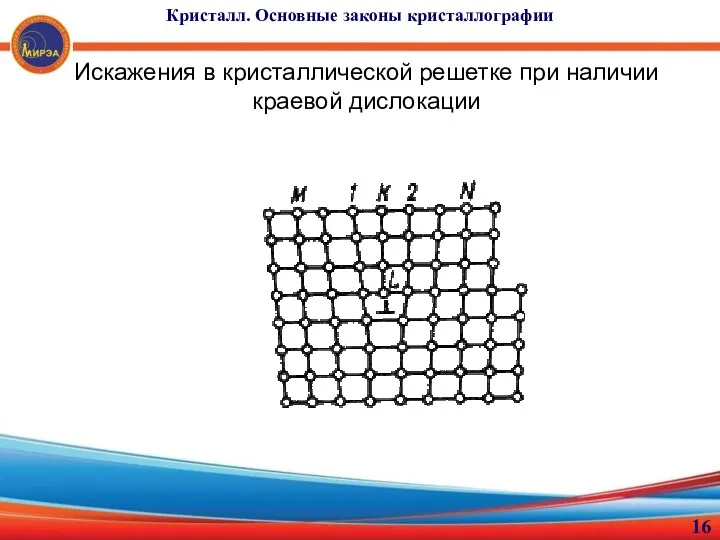
- 16. Кристалл. Основные законы кристаллографии Искажения в кристаллической решетке при наличии краевой дислокации
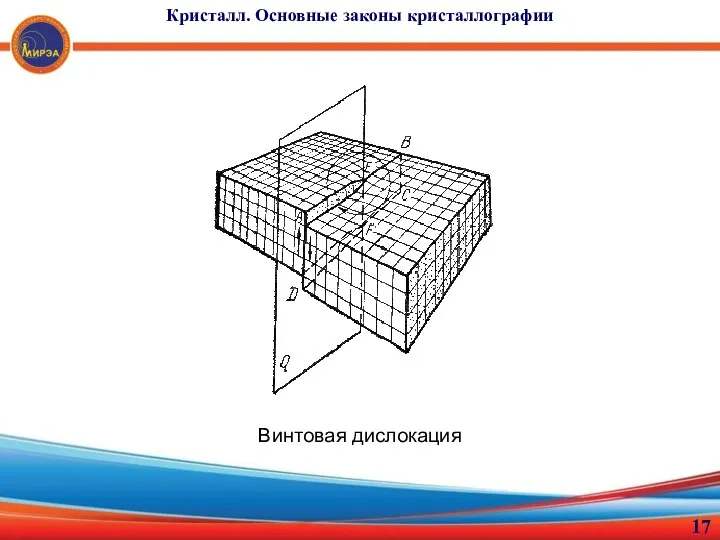
- 17. Винтовая дислокация Кристалл. Основные законы кристаллографии
- 18. Лекция 2 Кристаллографические категории и сингонии. Понятия о сингониях. Кристаллографические категории. Простые формы кристаллов. Кристаллографические категории
- 19. Сингония - классификация кристаллографических групп симметрии, кристаллов и кристаллических решёток в зависимости от системы координат (координатного
- 20. Кристаллографические категории и сингонии Характеристики координатных систем шести сингонии в трех кристаллографических категориях
- 21. Кристаллографические категории и сингонии Простые формы кристаллов Простой формой называется совокупность равных гpaнeй, связанных между собой
- 22. Кристаллографические категории и сингонии В названии простых форм используются греческие слова: моно – 1; ди –
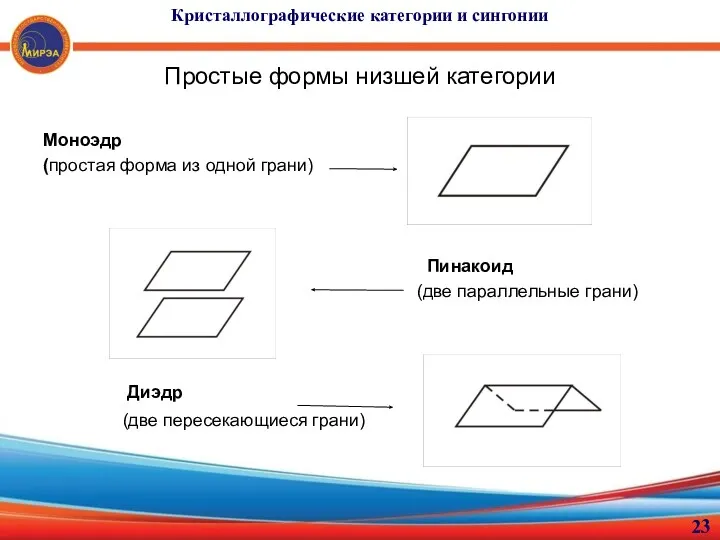
- 23. Кристаллографические категории и сингонии Простые формы низшей категории Моноэдр (простая форма из одной грани) Пинакоид (две
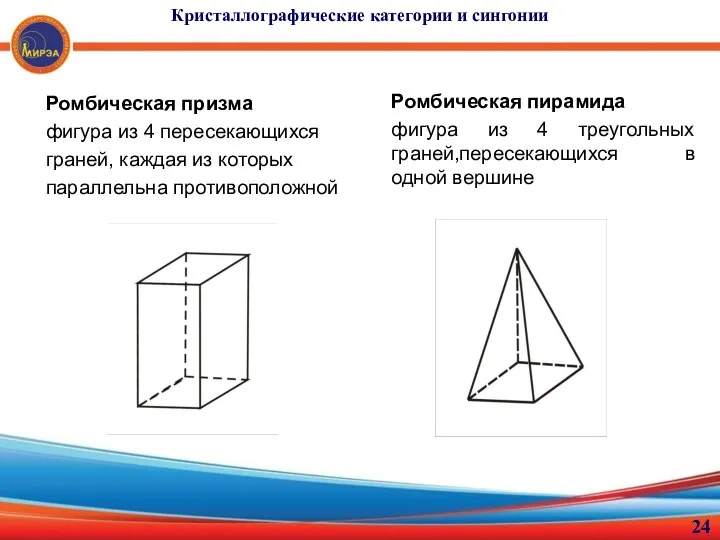
- 24. Кристаллографические категории и сингонии Ромбическая призма фигура из 4 пересекающихся граней, каждая из которых параллельна противоположной
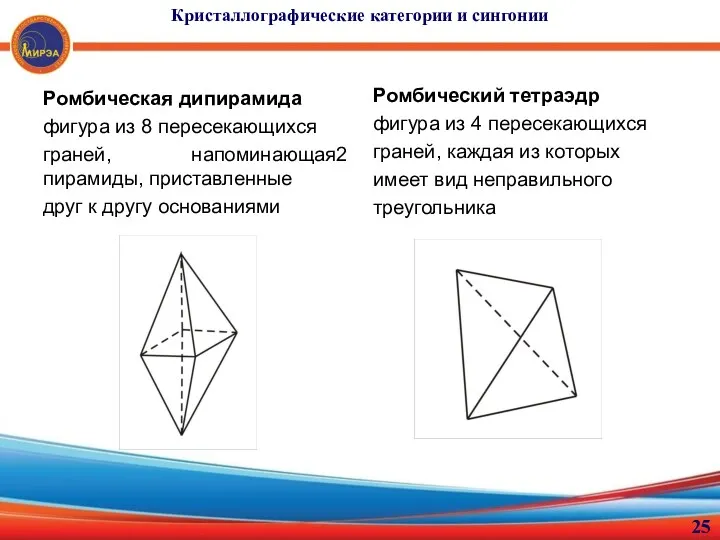
- 25. Кристаллографические категории и сингонии Ромбическая дипирамида фигура из 8 пересекающихся граней, напоминающая2 пирамиды, приставленные друг к
- 26. Кристаллографические категории и сингонии Простые формы средней категории Призмы представляют собой фигуры из прямоугольных пересекающихся граней,
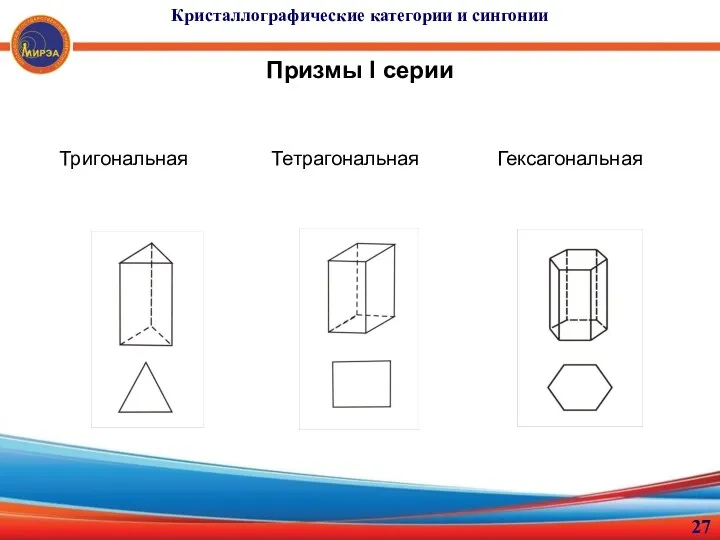
- 27. Кристаллографические категории и сингонии Призмы I серии Тригональная Тетрагональная Гексагональная
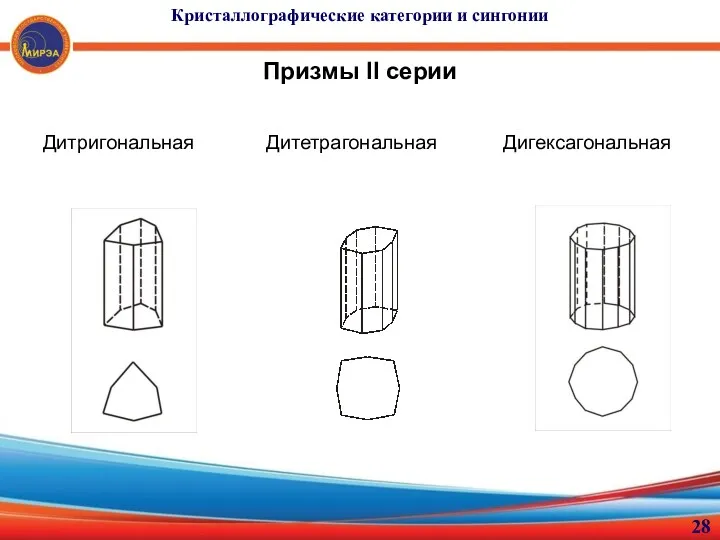
- 28. Кристаллографические категории и сингонии Призмы II серии Дитригональная Дитетрагональная Дигексагональная
- 29. Пирамиды - многогранники из треугольных пересекающихся граней, ребра которых сходятся в одной вершине. Дипирамиды - представляют
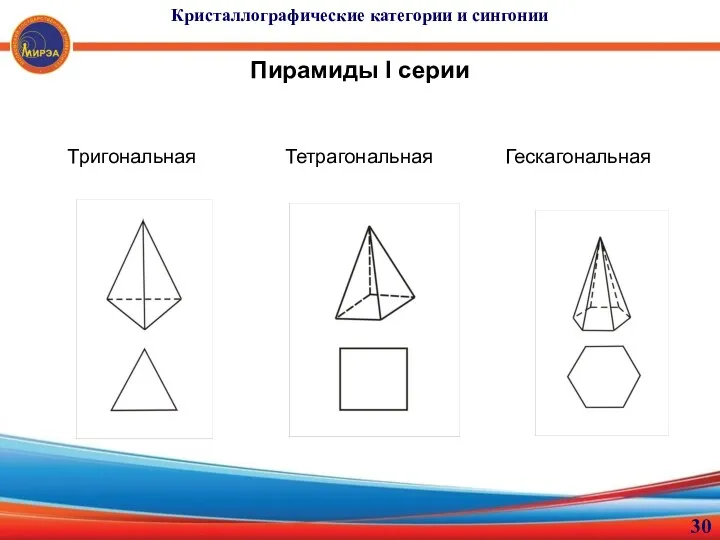
- 30. Кристаллографические категории и сингонии Пирамиды I серии Тригональная Тетрагональная Гескагональная
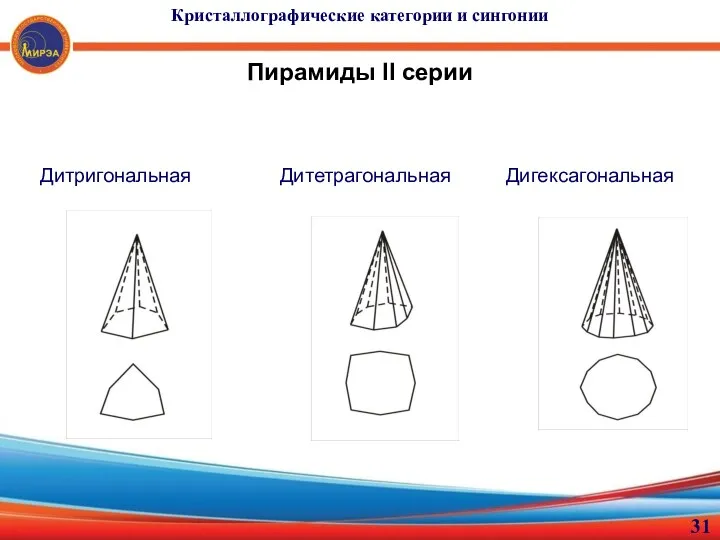
- 31. Дитригональная Дитетрагональная Дигексагональная Кристаллографические категории и сингонии Пирамиды II серии
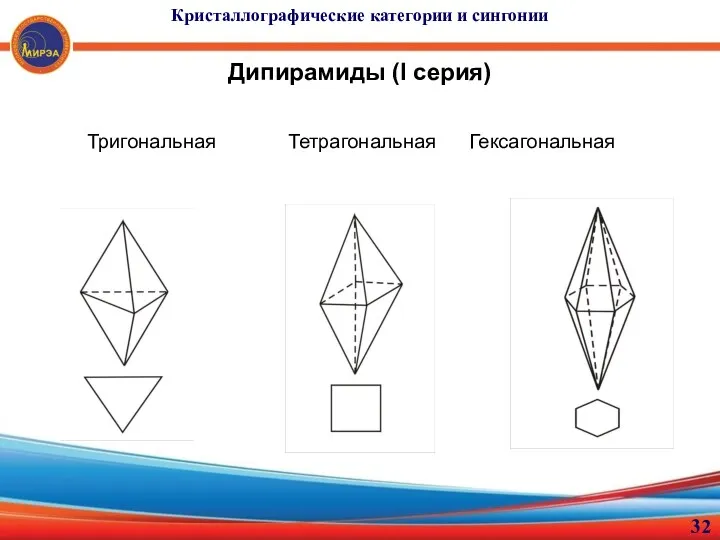
- 32. Кристаллографические категории и сингонии Дипирамиды (I серия) Тригональная Тетрагональная Гексагональная
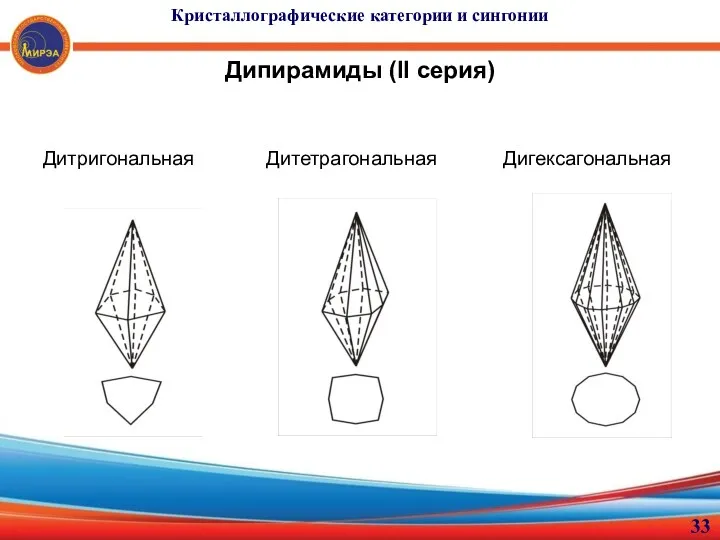
- 33. Кристаллографические категории и сингонии Дипирамиды (II серия) Дитригональная Дитетрагональная Дигексагональная
- 34. Кристаллографические категории и сингонии Тетраэдр - фигура из 4 пересекающихся граней, имеющих форму равнобедренных треугольников Ромбоэдр
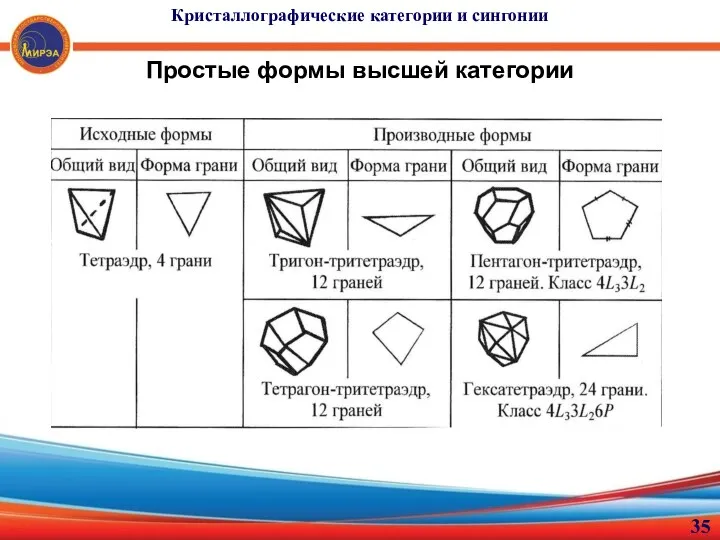
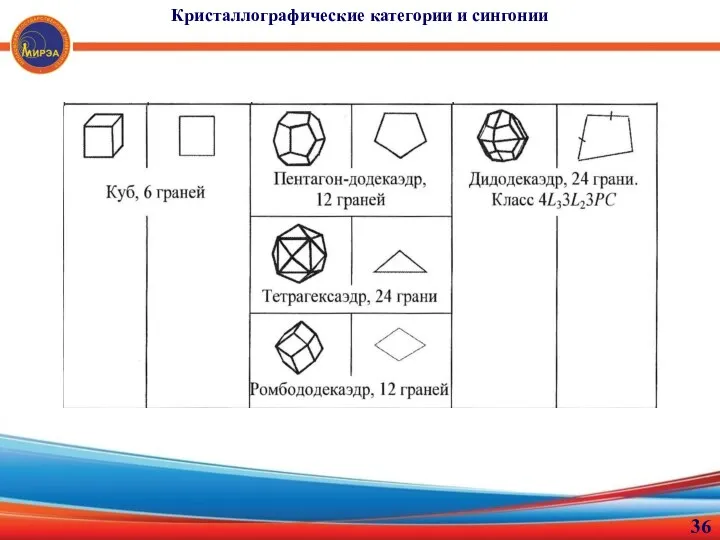
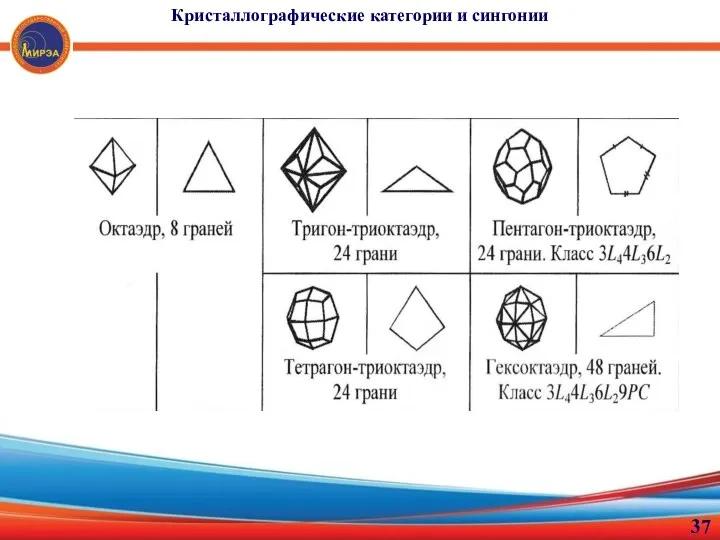
- 35. Кристаллографические категории и сингонии Простые формы высшей категории
- 36. Кристаллографические категории и сингонии
- 37. Кристаллографические категории и сингонии
- 38. Кристаллографические категории и сингонии Все простые формы принято разделять на открытые и закрытые. Открытые простые формы
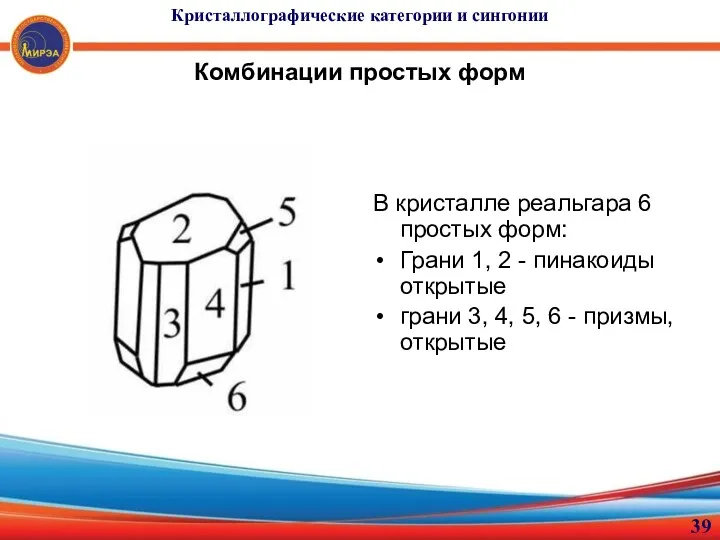
- 39. Кристаллографические категории и сингонии Комбинации простых форм В кристалле реальгара 6 простых форм: Грани 1, 2
- 40. Лекция 3 Элементы симметрии Основные понятия симметрии. Ось симметрии. Центр симметрии. Плоскость симметрии. Классы симметрии. Элементы
- 41. Симметрия (соразмерность, от лат. сим – одинаковый, метрос – размер) – правильная повторяемость элементов ограничения кристаллов
- 42. Элементами ограничения кристаллов считаются их грани, ребра и вершины. Симметрические операции – это повороты и отражения
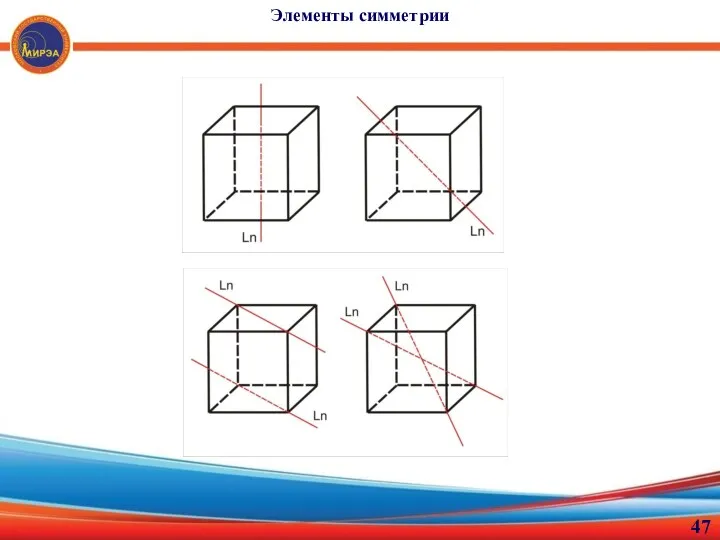
- 43. Ось симметрии Ln — прямая линия, при вращении вокруг которой повторяются равные части фигуры, то есть
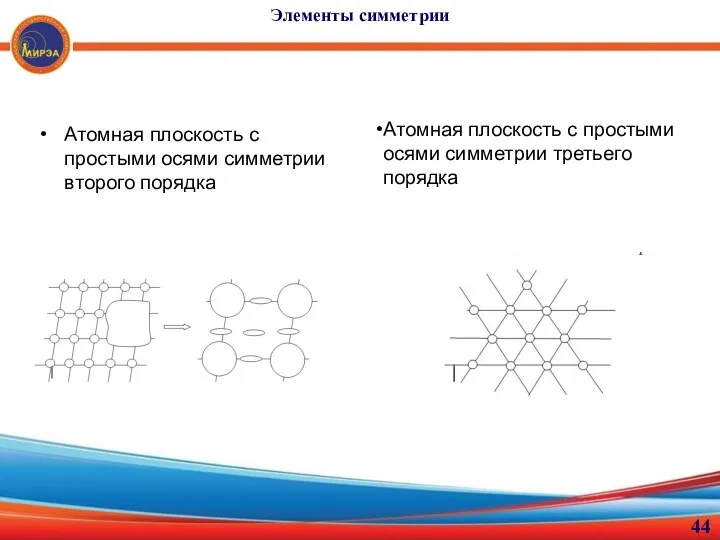
- 44. Элементы симметрии Атомная плоскость с простыми осями симметрии второго порядка Атомная плоскость с простыми осями симметрии
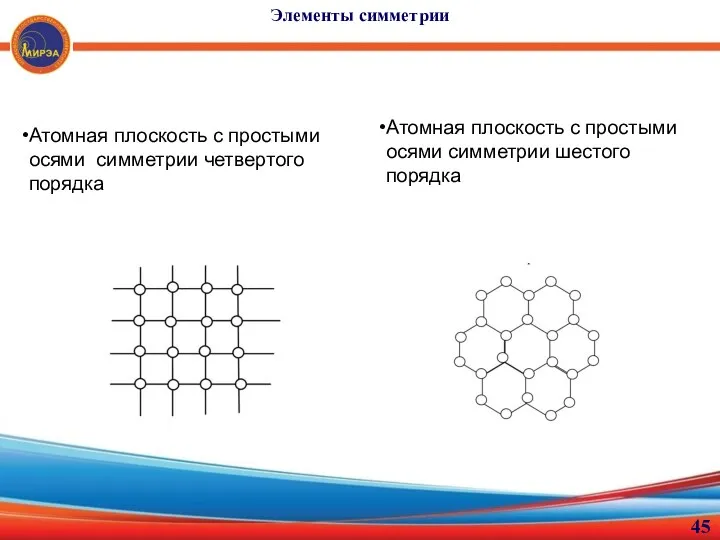
- 45. Элементы симметрии Атомная плоскость с простыми осями симметрии четвертого порядка Атомная плоскость с простыми осями симметрии
- 46. Основной закон кристаллографии В реальных кристаллах имеются оси симметрии первого L1, второго L2, третьего L3, четвертого
- 47. Элементы симметрии
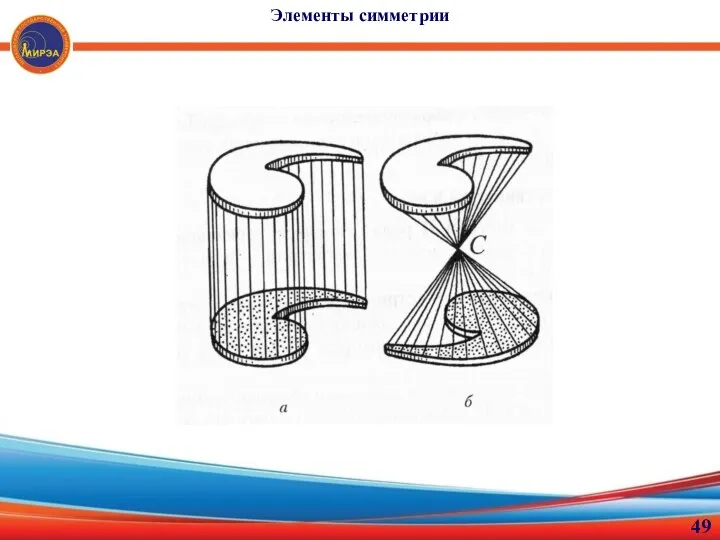
- 48. Центр симметрии (С) — это точка внутри кристалла, по обе стороны которой на равных расстояниях находятся
- 49. Элементы симметрии
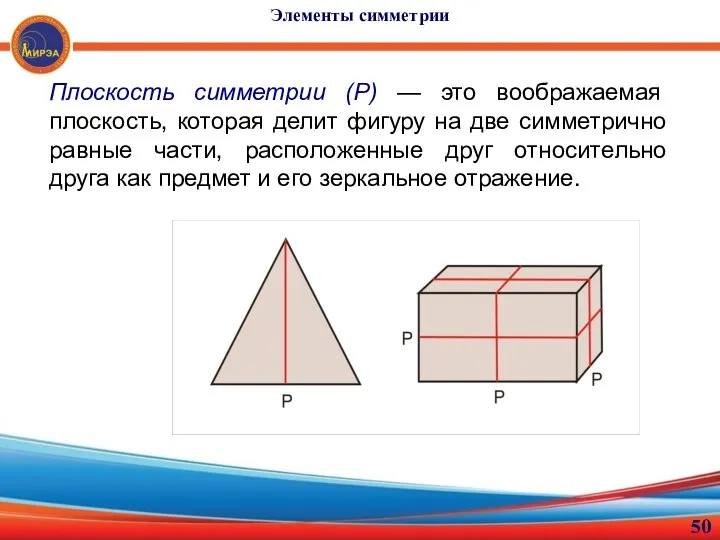
- 50. Плоскость симметрии (Р) — это воображаемая плоскость, которая делит фигуру на две симметрично равные части, расположенные
- 51. Элементы симметрии Классы симметрии средней и низшей категорий а) простейший; б) центральный; в) планальный; г) аксиальный;
- 52. Лекция 4 Кристаллографические проекции 1. Сферическая проекция. 2. Стереографическая проекция. 3. Гномостереографическая проекция. Кристаллографические проекции
- 53. Согласно закону постоянства углов, характерными параметрами любого кристаллического вещества являются углы между гранями (между определенными сетками
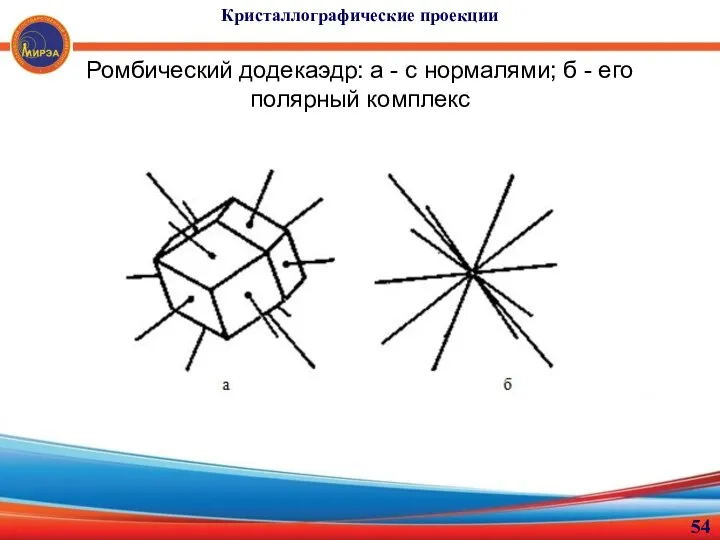
- 54. Кристаллографические проекции Ромбический додекаэдр: а - с нормалями; б - его полярный комплекс
- 55. Кристаллографические проекции Сферическая проекция Принцип построения сферической проекции.
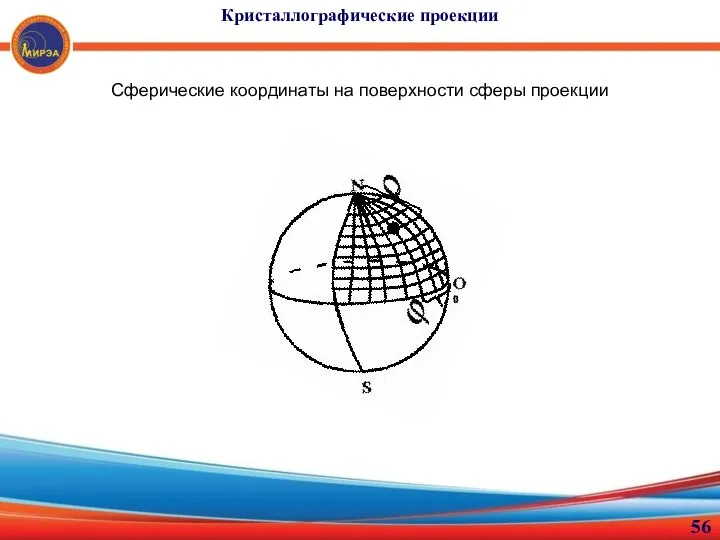
- 56. Кристаллографические проекции Сферические координаты на поверхности сферы проекции
- 57. Кристаллографические проекции Стереографическая проекция Принцип построения стереографической проекции
- 58. Кристаллографические проекции Построение стереографической проекции a, b, d плоскости R
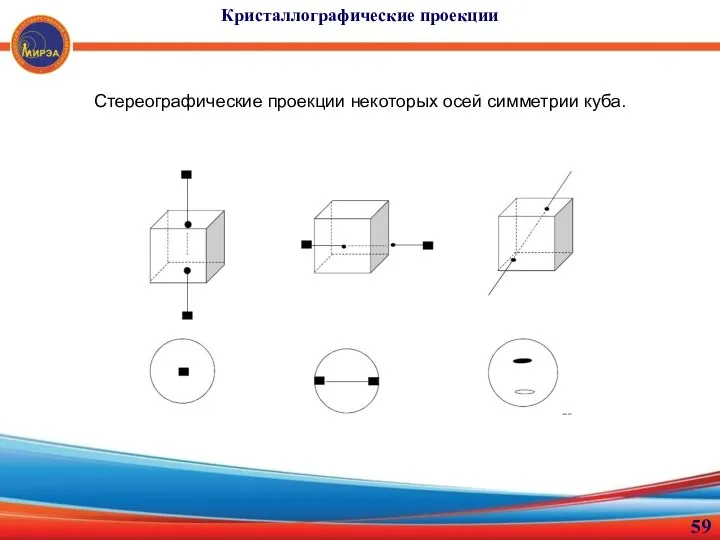
- 59. Кристаллографические проекции Стереографические проекции некоторых осей симметрии куба.
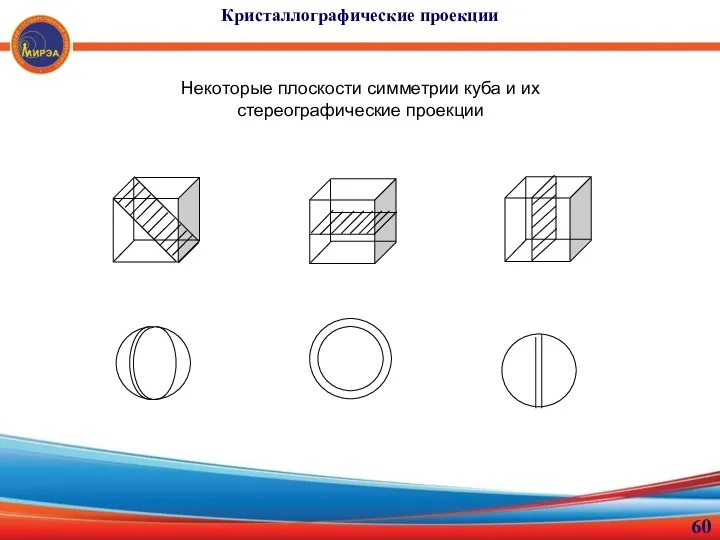
- 60. Кристаллографические проекции Некоторые плоскости симметрии куба и их стереографические проекции
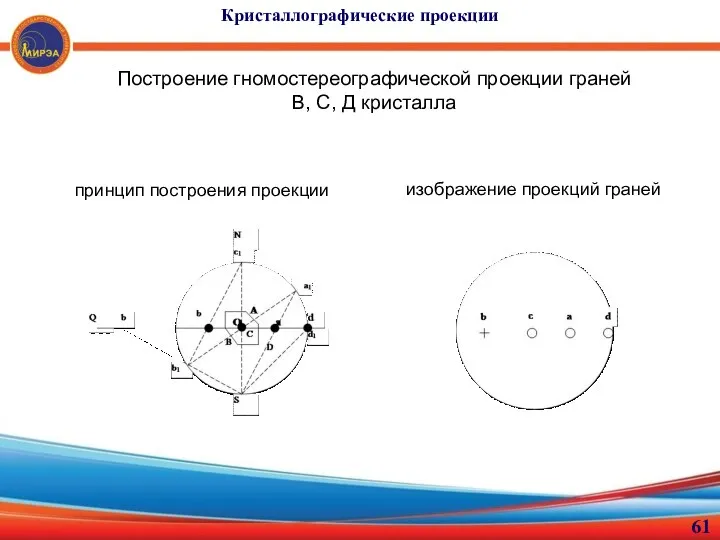
- 61. Кристаллографические проекции Построение гномостереографической проекции граней В, С, Д кристалла принцип построения проекции изображение проекций граней
- 62. Лекция 5 Теория плотнейших шаровых упаковок Основные принципы шаровой укладки. Разделение плотнейших шаровых укладок. Тыпы пустот
- 63. Теория плотнейших шаровых упаковок Плотнейшая шаровая укладка из квадратных слоев: а — изолированный квадратный шаровой слой
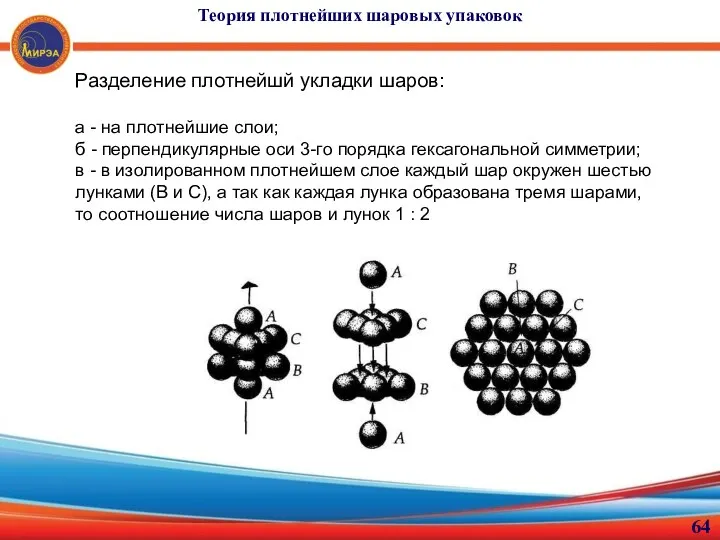
- 64. Теория плотнейших шаровых упаковок Разделение плотнейшй укладки шаров: а - на плотнейшие слои; б - перпендикулярные
- 65. Теория плотнейших шаровых упаковок Шары 2-го слоя заполняют лишь половину лунок предыдущего плотноупакованного слоя. Образуется половина
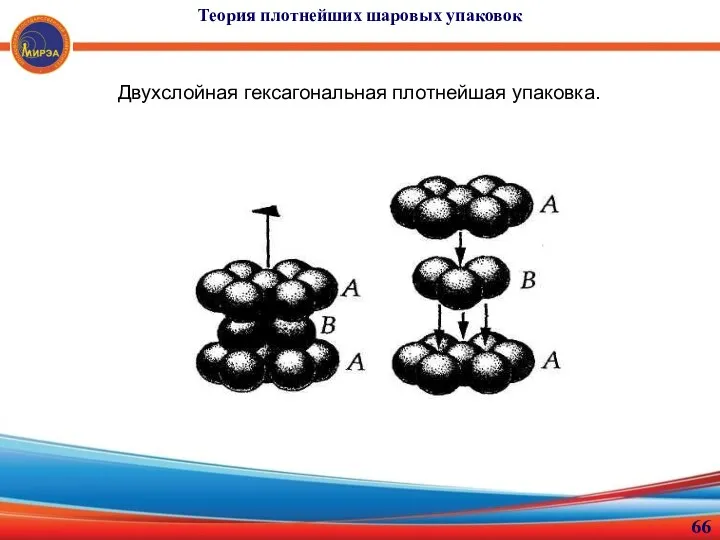
- 66. Теория плотнейших шаровых упаковок Двухслойная гексагональная плотнейшая упаковка.
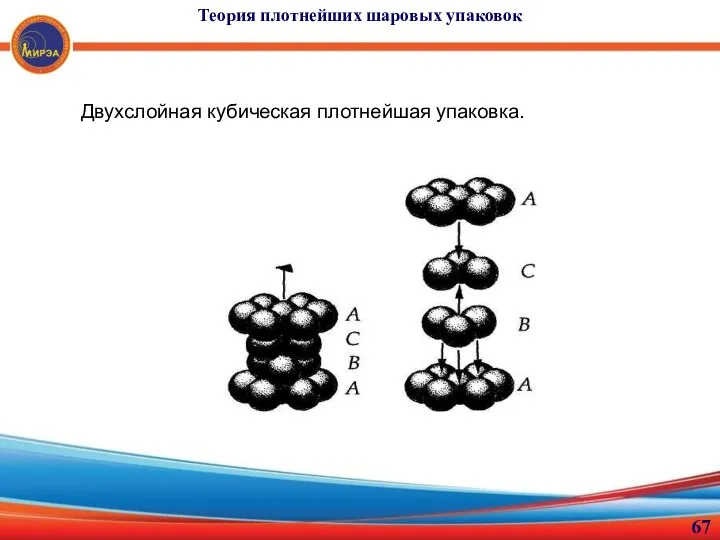
- 67. Теория плотнейших шаровых упаковок Двухслойная кубическая плотнейшая упаковка.
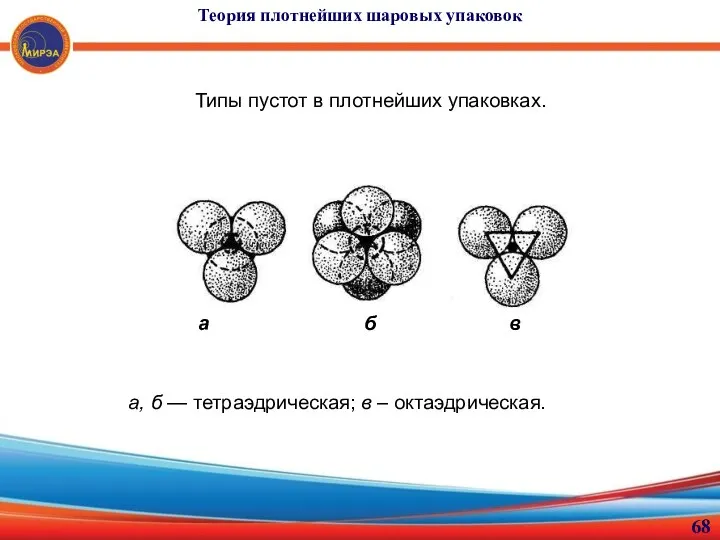
- 68. Теория плотнейших шаровых упаковок Типы пустот в плотнейших упаковках. а, б — тетраэдрическая; в – октаэдрическая.
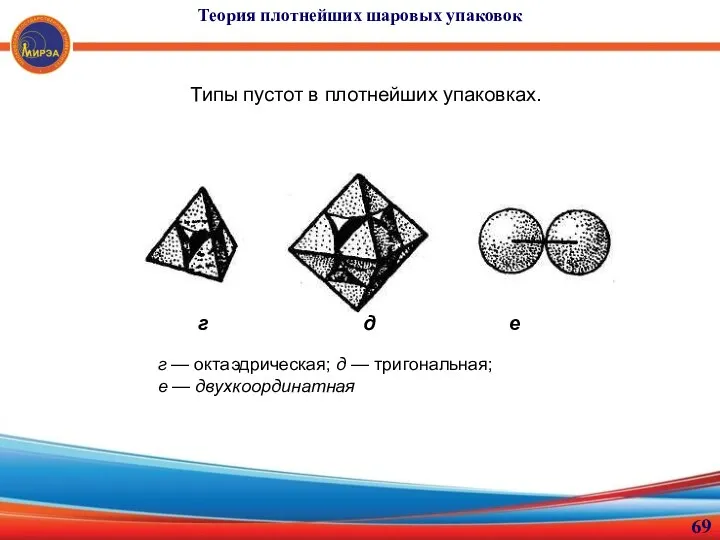
- 69. Теория плотнейших шаровых упаковок Типы пустот в плотнейших упаковках. г д е г — октаэдрическая; д
- 70. Лекция 6 Основы кристаллохимии 1.Радиусы атомные и ионные. 2.Типы химических связей. 3. Изоморфизм и полиморфизм. Основы
- 71. Кристаллохимия - изучает связь между атомным строением (структурой) кристаллов и их химическими, физическими и геометрическими свойствами.
- 72. Атомные и ионные радиусы – это минимальное расстояние, на которое центр сферы данного атома (иона) может
- 73. Основы кристаллохимии Во время роста кристаллов ионы, слагающие минерал, стремятся заполнить пространство наиболее экономичным образом, то
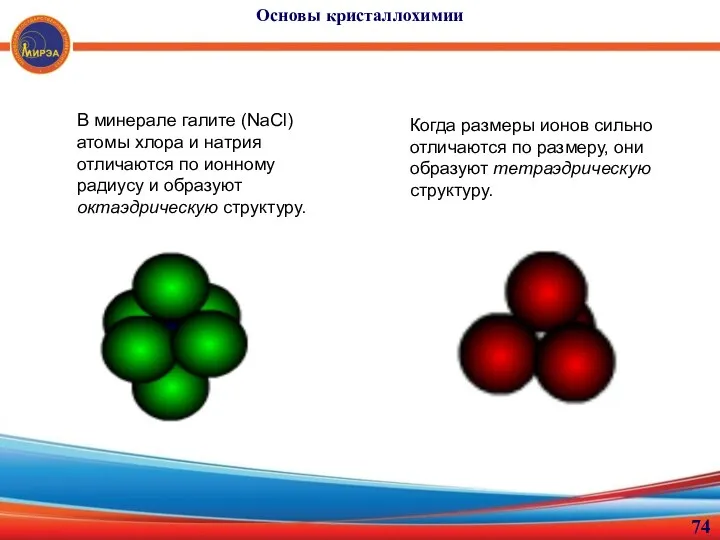
- 74. Основы кристаллохимии В минерале галите (NaCl) атомы хлора и натрия отличаются по ионному радиусу и образуют
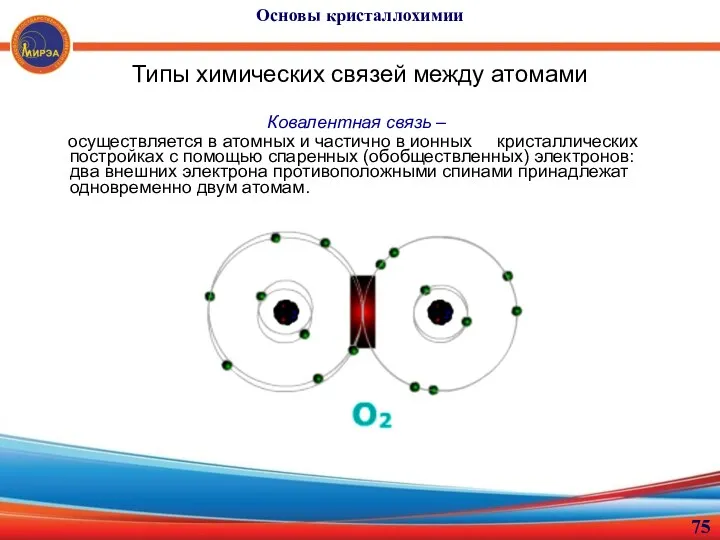
- 75. Основы кристаллохимии Типы химических связей между атомами Ковалентная связь – осуществляется в атомных и частично в
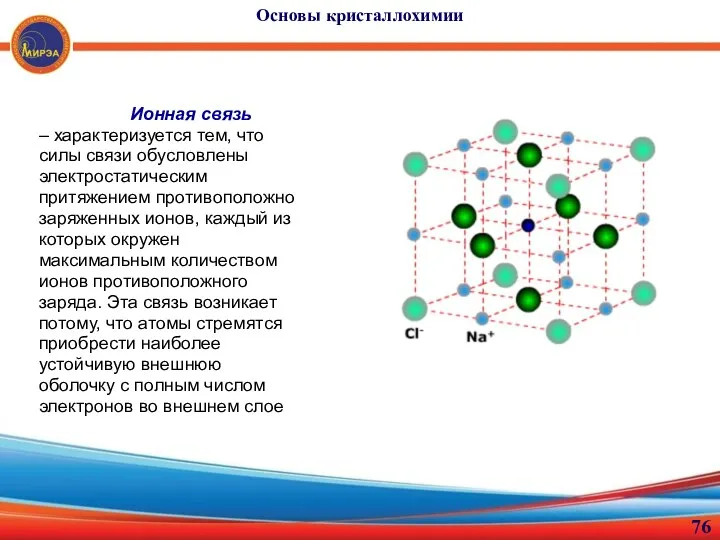
- 76. Основы кристаллохимии Ионная связь – характеризуется тем, что силы связи обусловлены электростатическим притяжением противоположно заряженных ионов,
- 77. Основы кристаллохимии Металлическая связь характерна для атомов металлов, которые имеют тенденцию легко расставаться с электронами внешней
- 78. Изоморфизм (от греч. «изос» — равный, «морфэ» — форма) - явление взаимного замещения атомов, ионов или
- 79. Основы кристаллохимии Виды изоморфизма 1. Совершенный (неограниченный) изоморфизм – это явление полного без ограничений замещения, т.е.
- 80. Полиморфизм (от греч. «поли» — много, «морфэ» — форма) - свойство соединений и простых веществ в
- 81. Полиморфные превращения – переходы из одной кристаллической формы в другую. Устойчивые в тех или иных термодинамических
- 82. Основы кристаллохимии Пример полиморфизма
- 83. Лекция 7 Образование и рост кристаллов. Моделирование процесса роста кристалла. Оптимизация режимов роста кристаллов. Процесс кристаллизации
- 84. Задачи моделирования роста кристаллов: расплавление шихты; затравливание; разращивание; рост вертикальной части; завершение; охлаждение. Образование и рост
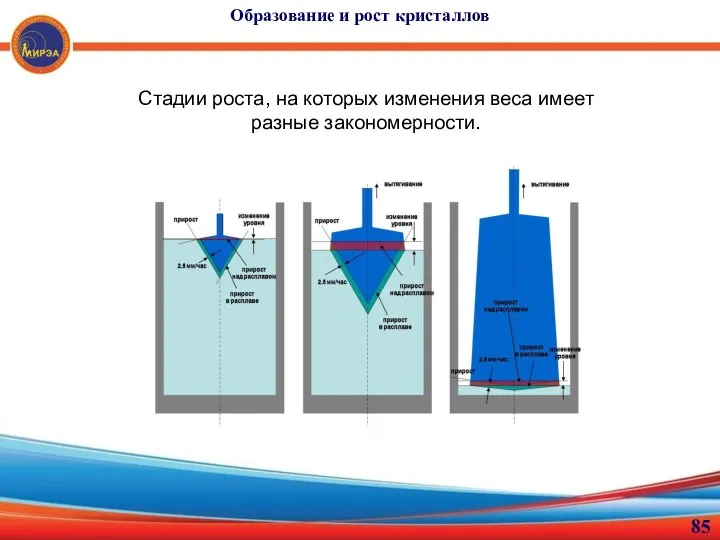
- 85. Образование и рост кристаллов Стадии роста, на которых изменения веса имеет разные закономерности.
- 86. Образование и рост кристаллов Выращенные кристаллы
- 87. Образование и рост кристаллов Фото образцов кернов
- 88. Образование и рост кристаллов Схема процесса кристаллизации металла
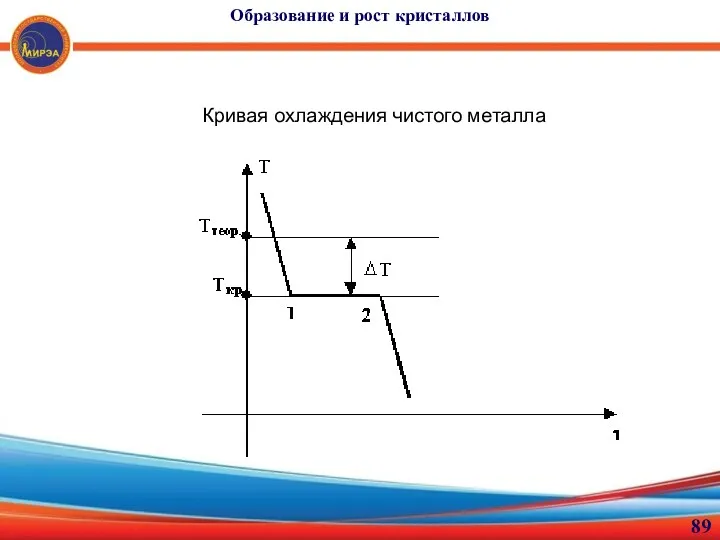
- 89. Образование и рост кристаллов Кривая охлаждения чистого металла
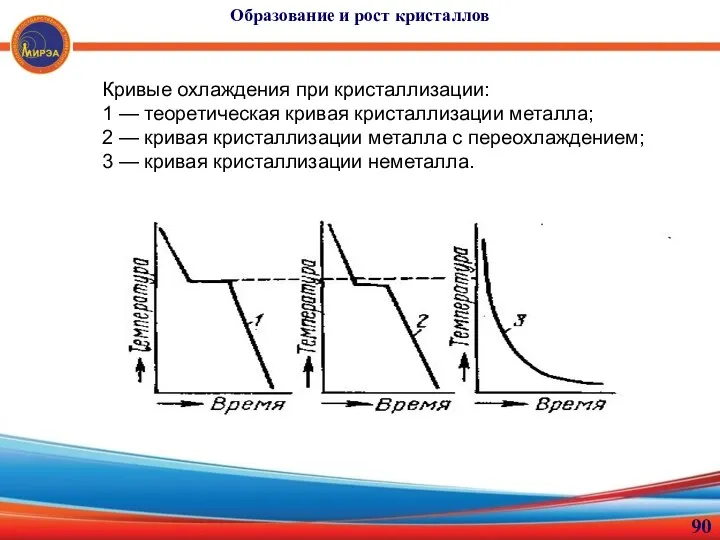
- 90. Образование и рост кристаллов Кривые охлаждения при кристаллизации: 1 — теоретическая кривая кристаллизации металла; 2 —
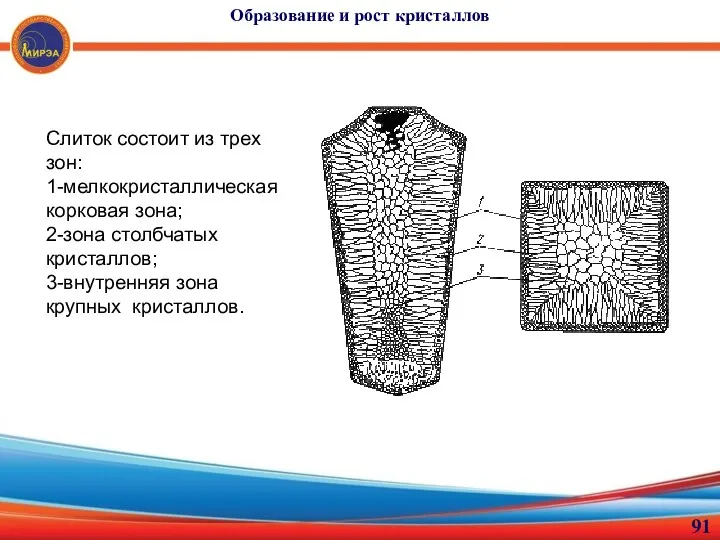
- 91. Образование и рост кристаллов Слиток состоит из трех зон: 1-мелкокристаллическая корковая зона; 2-зона столбчатых кристаллов; 3-внутренняя
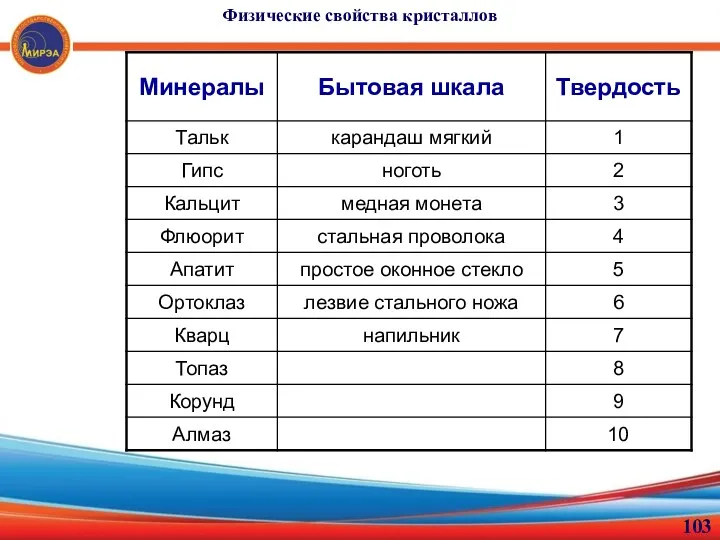
- 92. Лекция 8 Физические свойства кристаллов Механические свойства кристаллов. Оптические свойства кристаллов. Физические свойства кристаллов
- 93. Физические свойства кристаллов представлены механическими, оптическими, электрическими и пр. свойствами кристаллов. Обусловлены основными свойствами кристаллического вещества:
- 94. Механические свойства кристаллов Спайностью называется свойство кристаллов раскалываться или расщепляться по определенным кристаллографическим направлениям с образованием
- 95. Физические свойства кристаллов В зависимости от степени совершенства выделяют несколько видов спайности Весьма совершенная спайность –
- 96. Физические свойства кристаллов Несовершенная спайность обнаруживается с трудом, ее нужно искать на обломке минерала. Изломы представляют
- 97. Физические свойства кристаллов Весьма несовершенная спайность Практически отсутствует. Такие тела имеют раковистый излом (подобно обсидиану).
- 98. Излом – способность минералов раскалываться не по плоскостям спайности, а по сложной неровной поверхности. Физические свойства
- 99. Физические свойства кристаллов Раковистый излом похож на внутреннюю поверхность раковины, характерен для кристаллов, у которых отсутствует
- 100. Физические свойства кристаллов Крючковатый излом поверхность излома как бы покрыта мелкими Крючочками (самородная медь, серебро и
- 101. Физические свойства кристаллов Ступенчатый излом для кристаллов со спайностью в нескольких направлениях, например, полевой шпат.
- 102. Магнитность – способность некоторых минералов действовать на магнитную стрелку компаса (сильно отклоняя ее) или притягиваться магнитом
- 103. Физические свойства кристаллов
- 104. Физические свойства кристаллов Оптические свойства кристаллов Прозрачность – способность минерала пропускать свет. В зависимости от степени
- 105. Физические свойства кристаллов Типы окраски минералов Идиохроматическая (от греческого идиос – собственный) – минерал имеет отчетливо
- 106. Физические свойства кристаллов Аллохроматическая (от греческого аллос - чужой) – минерал окрашен примесями Агат + Fe
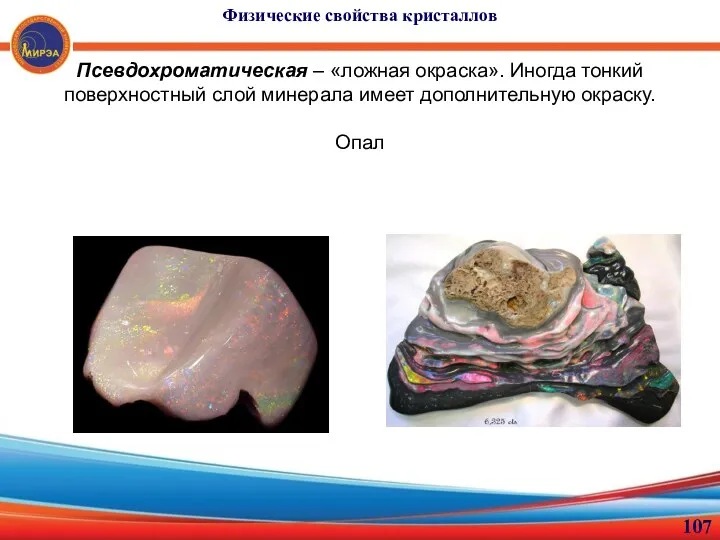
- 107. Физические свойства кристаллов Псевдохроматическая – «ложная окраска». Иногда тонкий поверхностный слой минерала имеет дополнительную окраску. Опал
- 108. Физические свойства кристаллов Блеск – способность минералов с различной интенсивностью отражать падающий на них свет Металлический
- 109. Физические свойства кристаллов в Полуметаллический блеск – более тусклый чем металлический, как у потускневших от времени
- 110. Физические свойства кристаллов в Стеклянный – поверхность минерала блестит как стекло. Стеклянным блеском обладает большинство (около
- 111. Физические свойства кристаллов в Шелковистый – обусловлен волокнистым строением минерала, поэтому минерал блестит и переливается, как
- 112. Физические свойства кристаллов в Жирный – поверхность минерала кажется смазанной жиром или покрытой маслянистой пленкой (нефелин,
- 113. Физические свойства кристаллов в Смоляной – блеск, напоминающий блеск застывшей смолы или гудрона (обсидиан, янтарь). Аналог
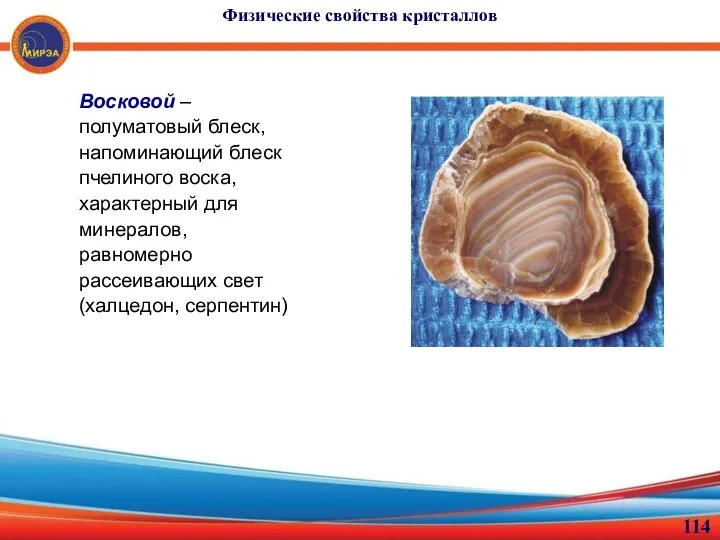
- 114. Физические свойства кристаллов в Восковой – полуматовый блеск, напоминающий блеск пчелиного воска, характерный для минералов, равномерно
- 115. Физические свойства кристаллов в Двупреломление – разложение в анизотропных средах светового луча, входящего в кристалл на
- 117. Скачать презентацию




































































 Types of chemical bonds in crystals
Types of chemical bonds in crystals Индикаторные ошибки кислотно-основного титрования
Индикаторные ошибки кислотно-основного титрования Подгруппа азота
Подгруппа азота Материаловедение. Контрольная работа
Материаловедение. Контрольная работа Вода - розчинник. Урок 41
Вода - розчинник. Урок 41 Щелочные металлы
Щелочные металлы Жорсткість води і методи її усунення. 11 клас
Жорсткість води і методи її усунення. 11 клас Тағам қоспалары
Тағам қоспалары Оксиды в минералогии
Оксиды в минералогии Классификация минералов по химическому принципу. Занятие 14
Классификация минералов по химическому принципу. Занятие 14 Закон сохранения массы вещества. Уравнения химических
Закон сохранения массы вещества. Уравнения химических Строение и свойства циклоалканов
Строение и свойства циклоалканов Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Галогены
Галогены Алюминий и его соединения
Алюминий и его соединения Решение экспериментальных задач по теме Металлы и их соединения. Практическая работа №4
Решение экспериментальных задач по теме Металлы и их соединения. Практическая работа №4 Chemistry of Coordination Compounds
Chemistry of Coordination Compounds Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью
Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью Знаки химических элементов. Химические формулы. Химический диктант
Знаки химических элементов. Химические формулы. Химический диктант kremniy
kremniy Соли, их классификация и свойства
Соли, их классификация и свойства Коллоидная химия
Коллоидная химия Тема 6-Альдегиды и кетоны
Тема 6-Альдегиды и кетоны Хімія і здоров'я людини
Хімія і здоров'я людини Особенности строения соединений органической химии. 10 класс
Особенности строения соединений органической химии. 10 класс Металлы главных подгрупп
Металлы главных подгрупп 20230419_soli
20230419_soli Агрегатные состояния вещества
Агрегатные состояния вещества