Получение
Как правило, исходным материалом для производства титана и его соединений служит
диоксид титана со сравнительно небольшим количеством примесей. В частности, это может быть рутиловый концентрат, получаемый при обогащении титановых руд. Однако запасы рутила в мире весьма ограничены, и чаще применяют так называемый синтетический рутил или титановый шлак, получаемые при переработке ильменитовых концентратов. Для получения титанового шлака ильменитовый концентрат восстанавливают в электродуговой печи, при этом железо отделяется в металлическую фазу (чугун), а невосстановленные оксиды титана и примесей образуют шлаковую фазу. Богатый шлак перерабатывают хлоридным или сернокислотным способом.
04.12.2017




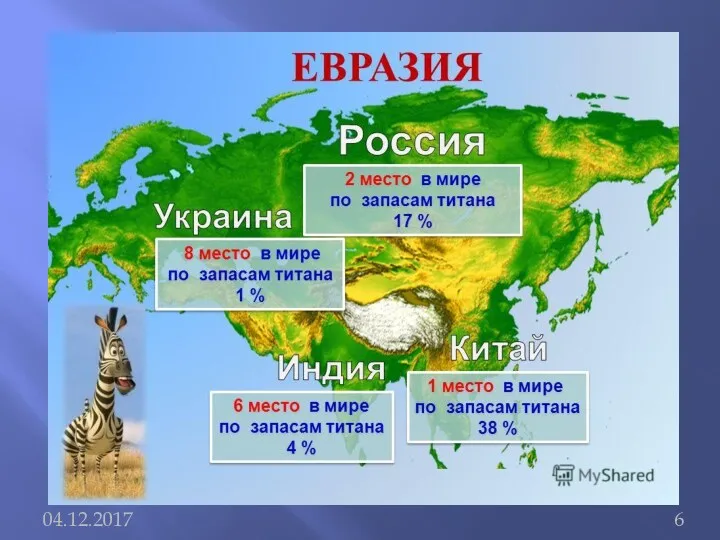
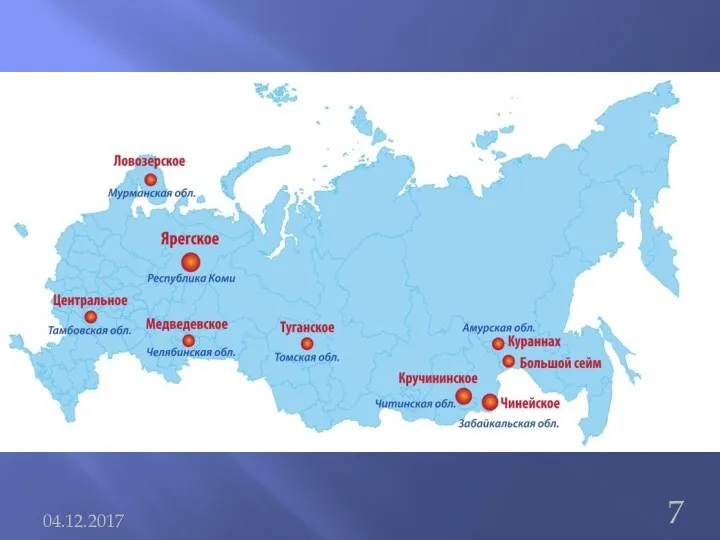





 Хром
Хром Металлы. Лекция № 9
Металлы. Лекция № 9 Решение упражнений по теме: Углеводы
Решение упражнений по теме: Углеводы Контрольная работа. Разбор. 9 класс
Контрольная работа. Разбор. 9 класс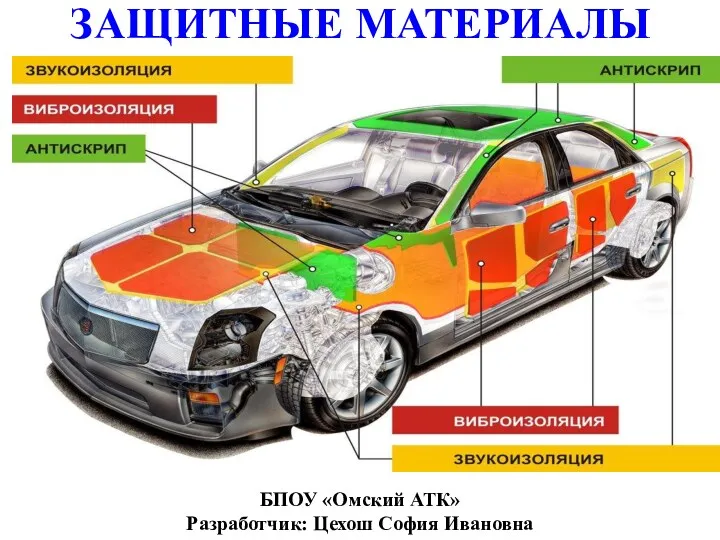 Защитные материалы
Защитные материалы Магнитные наночастицы: проблемы и достижения
Магнитные наночастицы: проблемы и достижения Кислотно-основные равновесия в водном растворе. Буферные растворы. (Лекция 3)
Кислотно-основные равновесия в водном растворе. Буферные растворы. (Лекция 3) Палладий. История открытия химических веществ
Палладий. История открытия химических веществ Общая характеристика неметаллов
Общая характеристика неметаллов Аммиак. Строение, свойства, получение, применение
Аммиак. Строение, свойства, получение, применение Оксиды. Понятия об оксидах
Оксиды. Понятия об оксидах Путешествие на остров Соединений химических элементов. Урок-игра
Путешествие на остров Соединений химических элементов. Урок-игра Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул
Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул Алюминий и его соединения
Алюминий и его соединения Растворы. (Лекция 7)
Растворы. (Лекция 7) Химические методы определения U, Pu, Th
Химические методы определения U, Pu, Th Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Химическое равновесие
Химическое равновесие d997-13229e5e
d997-13229e5e Типы химических реакций
Типы химических реакций Методы выделения и очистки продуктов биотехнологических производств
Методы выделения и очистки продуктов биотехнологических производств Соли аммония
Соли аммония Минералогический состав почв
Минералогический состав почв Physical chemistry of nanostructured systems
Physical chemistry of nanostructured systems Азотсодержащие органические соединения
Азотсодержащие органические соединения История развитии химии
История развитии химии Objectives and background. Apply for an unknown mixture
Objectives and background. Apply for an unknown mixture Аллотропные модификации кремния
Аллотропные модификации кремния