Содержание
- 2. Великие законы мирозданья в сущности, наивны и просты. И порой Вам не хватает знанья для разгадки
- 3. Прослушав легенду, попробуйте отгадать о каком элементе 3-й группы идет речь?
- 4. “Однажды к древнеримскому императору Тиберию правившему Римом в 14–27 гг. н. э., пришёл ремесленник и принёс
- 5. Как вы думаете о каком металле идет речь? Верно! Речь сегодня пойдет, ОБ АЛЮМИНИИ
- 6. Тема урока: «Алюминий и его свойства» 30.10.13г.
- 7. В результате изучения темы вы будете способны: Давать хар-ку алюминия как хим.элементу по ПСХЭ Давать хар-ку
- 8. I. Характеристика химического элемента: 1.Порядковый номер 2.Относительная атомная масса 3.Заряд ядра атома 4.Число протонов 5.Число электронов
- 9. II.Нахождение в природе По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния
- 10. ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ АЛЮМОСИЛИКАТЫ КОРУНД Al2O3 – прозрачные кристаллы
- 11. III. Получение алюминия: Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы
- 12. 2Al2O3 4Al + 3O2 эл.ток
- 13. IV. Физические свойства алюминия: Агрегатное состояние Цвет Блеск Плотность Твердость Пластичность Прочность Растворение в воде Теплопроводность
- 14. IV. Физические свойства алюминия: Алюминий – металл серебристо- белого цвета, лёгкий ( q= 2,7 г/ см3),
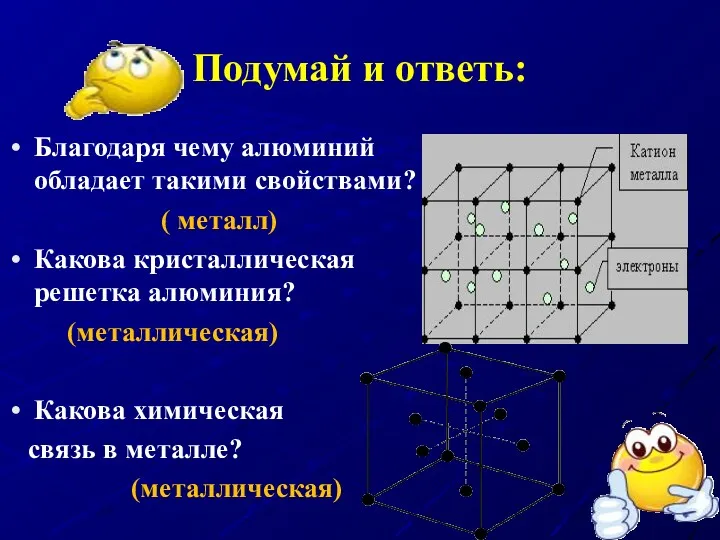
- 15. Подумай и ответь: Благодаря чему алюминий обладает такими свойствами? ( металл) Какова кристаллическая решетка алюминия? (металлическая)
- 16. V. Химические свойства алюминия: Алюминий – активный металл? Al ↔ Al +3 0 3 ē ок-ся
- 17. Ребята, берегите зрение! Ребята, берегите зрение!
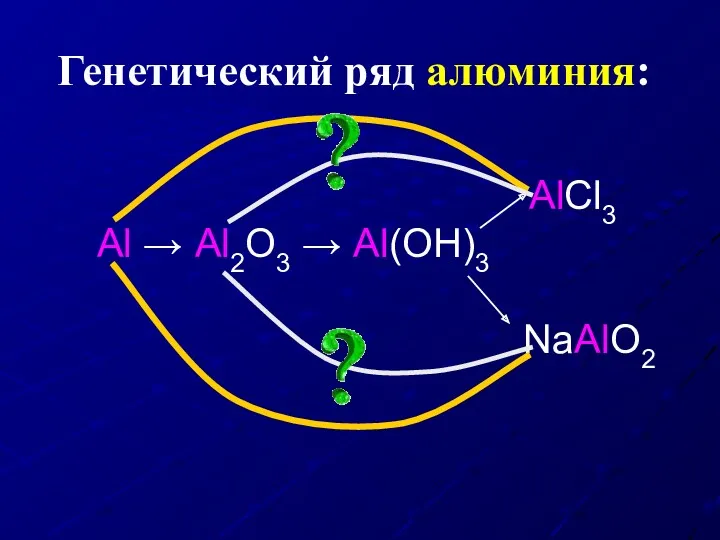
- 18. Генетический ряд алюминия: Al → Al2O3 → Al(OH)3 AlCl3 NaAlO2
- 19. (видео) 4Al+3O2 = 2Al2O3 (видео) 2Al+3Br2 = 2Al Br3 2 Al+3I2 = 2Al I3 2Al+3S =
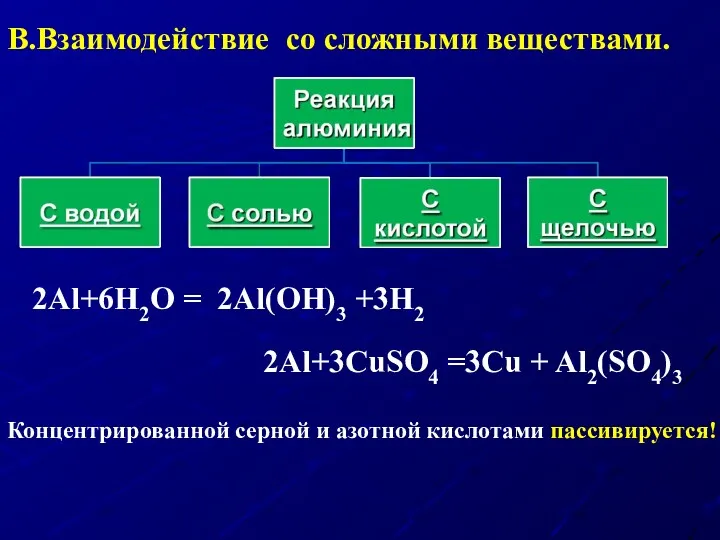
- 20. 2Al+3CuSO4 =3Cu + Al2(SO4)3 2Al+6Н2O = 2Al(OH)3 +3H2 Концентрированной серной и азотной кислотами пассивируется! В.Взаимодействие со
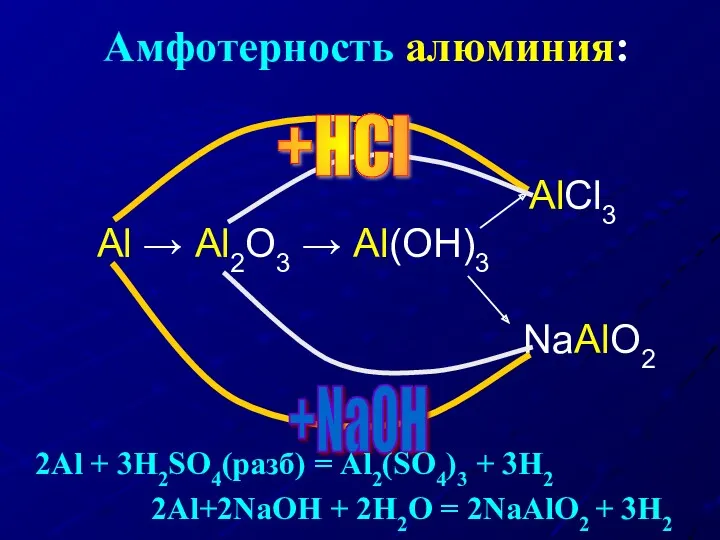
- 21. Амфотерность алюминия: Al → Al2O3 → Al(OH)3 AlCl3 NaAlO2 +HCl +NaOH 2Al + 3H2SO4(разб) = Al2(SO4)3
- 22. Активность алюминия Вывод: Алюминий - активный металл, реагирует со многими простыми и сложными веществами. В реакциях
- 23. VI. Применение алюминия для производства легких сплавов (дюралюмин, силумин) в самолето– и автомобилестроении для покрытия чугунных
- 24. NB!Сплавы на основе алюминия Алюминиево-магниевые Алюминиево-марганцевые Алюминиево-медные Сплавы системы Al-Zn-Mg Алюминиево-кремниевые сплавы (силумины) Комплексные сплавы на
- 25. Алюминий в мировой культуре Поэт Андрей Вознесенский написал в 1959 году стихотворение «Осень», в котором использовал
- 26. Алюминий в мировой культуре Виктор Цой написал песню «Алюминиевые огурцы» с припевом: Я сажаю алюминиевые огурцы
- 27. Токсичность Al Отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в
- 28. Экспресс- опрос 1.Сколько электронов на последней оболочке у атома алюминия. А.1 В.4 C. 3 D. 6
- 29. Подведем -итоги Над какой темой мы сегодня работали? Что нового мы узнали об алюминии? Решили ли
- 30. «Острова» о. Грусти О. Удовольствия о.Тревоги о.Просветления о. Воодушевления о.Неопределенности о. Недоумения о.Радости о.Бермудский треугольник
- 31. Домашнее задание Разобрать и выучить конспект. Выучить параграф: § 2.8 Выполнить упр: 1,3,2* стр. 51.
- 33. Скачать презентацию


























 Цинк. Месторождения. Применение
Цинк. Месторождения. Применение Азот қышқылы
Азот қышқылы Нафта. Класифікація нафти
Нафта. Класифікація нафти Кислородные соединения углерода
Кислородные соединения углерода Кислород
Кислород Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ
Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ Генетическая связь между классами веществ
Генетическая связь между классами веществ Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Строение атома
Строение атома Характеристика элементов VIII-Б группы. Семейство железа
Характеристика элементов VIII-Б группы. Семейство железа Углеводы. Моносахариды. Лекция 5
Углеводы. Моносахариды. Лекция 5 Дисперсные системы. Растворы
Дисперсные системы. Растворы Химические свойства солей
Химические свойства солей Закономерности химических реакций. (Лекция 3)
Закономерности химических реакций. (Лекция 3) Жескость воды
Жескость воды Альдегіди
Альдегіди Поверхностные явления
Поверхностные явления Радиогеохимия метаморфических процессов
Радиогеохимия метаморфических процессов Природные каменные материалы
Природные каменные материалы Халькогены. Кислород
Халькогены. Кислород Законы химии. Классы неорганических соединений
Законы химии. Классы неорганических соединений Отрицательное влияние азотных минеральных удобрений на почву
Отрицательное влияние азотных минеральных удобрений на почву Химическая технология ситаллов и композитов
Химическая технология ситаллов и композитов Biomass Feedstocks
Biomass Feedstocks Physiology lab
Physiology lab Химия 8 класс. Введение в химию
Химия 8 класс. Введение в химию Предмет и объекты исследования коллоидной химии. Лекция 01
Предмет и объекты исследования коллоидной химии. Лекция 01 Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение
Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение